
______
ASSEMBLÉE NATIONALE
CONSTITUTION DU 4 OCTOBRE 1958
TREIZIÈME LÉGISLATURE
Enregistré à la Présidence de l’Assemblée nationale le 25 mai 2010.
RAPPORT D’INFORMATION
DÉPOSÉ
PAR LA COMMISSION DES AFFAIRES EUROPÉENNES(1)
sur les transplantations d’organes
(E 4173),
ET PRÉSENTÉ
PAR MM. Jérôme LAMBERT et Didier QUENTIN,
Députés
——
La Commission des affaires européennes est composée de : M. Pierre Lequiller, président ; MM. Michel Herbillon, Jérôme Lambert, Thierry Mariani, Didier Quentin, vice-présidents ; M. Jacques Desallangre, Mme Marietta Karamanli, MM. Francis Vercamer, Gérard Voisin secrétaires ; M. Alfred Almont, Mme Monique Boulestin, MM. Pierre Bourguignon, Yves Bur, François Calvet, Christophe Caresche, Philippe Cochet, Bernard Deflesselles, Lucien Degauchy, Michel Delebarre, Michel Diefenbacher, Jean Dionis du Séjour, Marc Dolez, Daniel Fasquelle, Pierre Forgues, Jean-Claude Fruteau, Jean Gaubert, Hervé Gaymard, Guy Geoffroy, Mmes Annick Girardin, Anne Grommerch, Elisabeth Guigou, Danièle Hoffman-Rispal, MM. Régis Juanico, Marc Laffineur, Robert Lecou, Michel Lefait, Lionnel Luca, Philippe Armand Martin, Jean-Claude Mignon, Jacques Myard, Michel Piron, Franck Riester, Mmes Chantal Robin-Rodrigo, Valérie Rosso-Debord, Odile Saugues, MM. André Schneider, Philippe Tourtelier.
SOMMAIRE
___
Pages
I. UNE COMPÉTENCE ESSENTIELLEMENT NATIONALE ET POUR LAQUELLE UNE COOPÉRATION DIRECTE EST DÉJÀ ORGANISÉE, D’UNE PART, ENTRE CERTAINS ETATS ET, D’AUTRE PART, AU SEIN DU CONSEIL DE L’EUROPE 9
A. UN ENJEU MAJEUR DE SANTÉ PUBLIQUE ESSENTIELLEMENT GÉRÉ DANS UN CADRE NATIONAL 9
1. Un contexte général de pénurie 9
2. D’importantes différences d’approches nationales et de résultats 10
a) Des perceptions variables selon les pays 10
b) Deux catégories d’Etats membres en matière de consentement 12
c) Des résultats contrastés 12
3. Un point d’éclairage sur la France et l’Espagne 15
B. UNE INTERVENTION COMMUNAUTAIRE PRÉVUE PAR LE TRAITÉ, MAIS RÉCENTE, D’AMPLEUR ASSEZ RÉDUITE ET QUI DOIT TROUVER SA PLACE ENTRE DES COOPÉRATIONS DIRECTES ENTRE ETATS ET UNE ACTION TRÈS POSITIVE DU CONSEIL DE L’EUROPE 17
1. Une compétence communautaire récente et limitée 17
2. Des coopérations entre Etats membres directes, structurées, multilatérales et organisées depuis longtemps 18
3. Les recommandations du livre blanc d’Alliance O, regroupant sept Etats membres 19
4. Les instruments juridiques et interventions du Conseil de l’Europe, notamment dans la lutte contre le trafic international d’organes 20
II. LA PROPOSITION DE DIRECTIVE SUR LES TRANSPLANTATIONS D’ORGANES : UNE TEXTE D’ÉQUILIBRE, UTILE ET RESPECTUEUX DU PRINCIPE DE SUBSIDIARITÉ 23
A. LES RÉSULTATS DU TEST CONCERTÉ DE SUBSIDIARITÉ ORGANISÉ DANS LE CADRE DE LA COSAC 23
1. Un calendrier bref 23
2. L’absence de réserve à l’Assemblée nationale, comme au Sénat 23
3. L’absence d’opposition de presque toutes les autres assemblées des Etats membres 28
B. UN DISPOSITIF FAVORABLE CENTRÉ SUR LA QUALITÉ ET LA SÉCURITÉ DES ORGANES 29
1. Un schéma classique 29
a) Une prise en compte des travaux du Conseil de l’Europe et d’Alliance O 29
b) Un champ d’application qui couvre toutes les transplantation d’organes 29
c) La reprise du triptyque de base : autorité nationale de contrôle, contrôle des établissements de prélèvement, autorisation des centres de transplantation 30
d) Des dispositions relatives à la qualité et la sécurité des organes qui couvrent l’ensemble de la chaîne, du prélèvement jusqu’au suivi du bénéficiaire de la greffe comme du donneur vivant 30
e) Une nouvelle instance de comitologie 31
2. Des objectifs ambitieux et nécessaires 31
a) Un objectif partagé de sécurité et de qualité en faveur d’une convergence vers le haut des pratiques européennes 31
b) Une volonté de réduction de la pénurie moins réaliste 31
c) Une contribution réelle à la lutte contre les trafics d’organes 32
3. L’intervention, en complément, du plan d’action sur le don et la transplantation d’organes 32
C. UN TEXTE ÉQUILIBRÉ ET AMÉLIORÉ PAR LES TRAVAUX PRÉPARATOIRES QUI PEUT DONC ÊTRE APPROUVÉ 33
1. Une absence d’interférence avec les compétences des Etats membres en matière de choix bioéthiques 33
2. Des compléments utiles 34
3. Un dispositif qui ne crée pas de difficulté pour la France 35
a) Des dispositions qui n’entraînent pas de bouleversement 35
b) Des dispositions qui donnent la souplesse demandée à l’annexe sur la caractérisation des organes et des donneurs 35
TRAVAUX DE LA COMMISSION 37
ANNEXE : LISTE DES PERSONNES ENTENDUES PAR LES RAPPORTEURS ET REMERCIEMENTS 39
Mesdames, Messieurs,
Sans évoquer les pratiques très anciennes de la médecine antique, avec des tentatives de greffe de membres notamment à Rome ou les premières greffes connues de peau en Inde, deux siècles avant notre ère, la transplantation d’organes est l’un des progrès les plus spectaculaires du XXe siècle.
Elle a été permise par les acquis des expérimentations menées dès le XIXe siècle. En 1869, la couverture des plaies par des fragments d’épiderme est tentée par Reverdin, en France. S’agissant des animaux, la première greffe de cornée animale intervient en 1837 et on fait aussi des essais de suture sur la queue des rats.
Les premières expériences de greffe d’organes, reins et cœurs, sont menées dès les années 1900. Alexis Carrel, prix Nobel de Médecine en 1912, étudie notamment les transplantations sur le chien et identifie le problème, qui restera insoluble pendant des décennies, du rejet. En 1905, c’est la première greffe de cornée humaine, par Eduard Zirm, un autrichien. En 1906, une première expérience est tentée par Mathieu Jaboulay, pour greffer un rein de chèvre au coude d’une femme urémique. Plusieurs expériences similaires suivent, avec des reins d’origine porcine ou ovine, mais c’est toujours l’échec.
Pendant la première guerre mondiale, notamment grâce aux travaux d’Harold Gillies, des progrès interviennent en matière de transplantation de peau, ce qui ouvre la voie de la chirurgie réparatrice.
La première tentative de greffe d’un organe d’origine humaine qui a donné lieu à publication intervient plus tard, en 1933, en URSS, avec l’implantation d’un rein prélevé sur le corps d’un mort. Elle est réalisée par Serguey Voronov. C’est un échec.
C’est après la Seconde guerre mondiale que les principaux progrès interviennent. Deux pôles de compétences émergent d’abord : les Etats-Unis, notamment Boston, et la France.
La première greffe rénale avec donneur vivant, et apparenté, intervient en 1952 à Paris. Elle est réalisée par l’équipe du professeur Jean Hamburger. La survie est de vingt et un jours.
En 1954, en revanche, à Boston, l’équipe de Joseph Murray, Merrill et Harrison réussit la première greffe avec donneur vivant. Il n’y a pas de problème de rejet, puisqu’elle intervient entre deux jumeaux.
Le premier préalable à la réussite de la greffe, celui de la suture vasculaire, est surmonté.
Le deuxième, celui de l’immuno-suppression, l’est ensuite, à partir des travaux du professeur Jean Dausset, qui découvre les antigènes et le système HLA et publie ses premiers résultats en 1952. Pour que la greffe réussisse, deux solutions sont alors possibles : soit les cartes d'identité génétiques du donneur et du receveur sont les plus proches possibles ; soit il faut affaiblir le système immunitaire du receveur afin qu'il n'y ait pas de rejet. L’immuno-suppression apparaît, par irradiation totale, mais rapidement on rejette cette solution en raison de ses effets secondaires, ou par substances chimiques, notamment par corticoïdes.
En 1956, à Boston puis à Paris, sont effectuées des greffes entre faux jumeaux avec irradiation et corticoïdes.
Le troisième préalable, celui de la disponibilité, relative, des organes, est également franchi au cours de cette même décennie. L’école neurologique parisienne identifie l'état de mort cérébrale, ce qui permet d’envisager le prélèvement à cœur battant et le don d'organes.
Le dernier préalable, celui de la conservation des organes, est à son tour maîtrisé.
En 1955, l’américain Norman Shumway met au point le système de conservation à froid du cœur, pour opérer. Ensuite, les travaux de Collins puis de Belzer apportent des solutés de protection des organes prélevés.
Le développement des greffes est alors rapide à partir des années 1960.
En 1962, la collaboration entre les professeurs Dausset et Hamburger permet de réaliser la première greffe compatible rénale en France.
La greffe rénale étant maîtrisée, la première greffe hépatique est réalisée en 1963 à Denver. Après un échec en 1963, un premier succès est enregistré pour la greffe pulmonaire par Derom à Gand, en 1968. En 1966, c’est la première greffe pancréatique.
La première greffe cardiaque est pour sa part intervenue en 1967 en Afrique du Sud, par Christiaan Barnard, suivie en 1968 par celle réalisée à Paris par Christian Cabrol, la première en Europe.
De nouvelles substances chimiques immuno-suppresseurs sont découvertes, notamment la cyclosporine en 1970.
Le domaine se développe, touche un plus grand nombre de patients et son champ s’accroît.
Il quitte ainsi les organes internes avec la première transplantation de trachée en 1979, du larynx en 1998 aux Etats-Unis, puis, de manière plus proche, la première greffe des deux mains réalisée en 2000 par l’équipe de notre ancien collègue député, le professeur Jean-Michel Dubernard, et celle du visage, en 2005, réalisée cette fois en collaboration avec l’équipe du professeur Bernard Devauchelle. En 2008, une greffe des deux bras est réalisée à Munich et en 2009, celle du visage et des mains, à l’hôpital de Créteil, par le professeur Laurent Lantiéri et les docteurs Jean-Paul Méningaud et Christian Dumontier.
Depuis, onze greffes du visage ont été réalisées. La dernière en date est une greffe totale du visage, réalisée à Barcelone, cette année.
Maintenant, la technique de la greffe est largement diffusée dans le monde et n’est plus l’apanage de quelques rares établissements dans les pays les plus développés, même si elle y est plus fréquente qu’ailleurs.
Le volume 14 no 1 de la lettre d’information Newsletter Transplant (septembre 2009) mentionne pour 2007, au titre des statistiques internationales, un total de 99 321 greffes d’organes, dont 68 250 greffes rénales, parmi lesquelles 45 % sur donneur vivant, 19 850 greffes de foie, 5 179 greffes de cœur, 3 245 greffes de rein et 2 797 greffes de pancréas.
La répartition géographique est éclairante avec environ 28 000 greffes pour les Etats-Unis et 17 000 pour l’Union européenne, et 8 800 pour l’Amérique latine.
L’un des principaux freins au développement des greffes d’organes, dont l’enjeu est essentiel, puisqu’il s’agit de la vie, est le manque de disponibilité des organes.
Il s’ensuit une situation paradoxale où les échanges légaux transfrontaliers d’organes sont extrêmement limités, et se réduisent à quelques unités pour la France, mais où une coopération internationale est nécessaire, pour éviter les trafics d’organes et faire respecter les principes éthiques fondamentaux qui sont à la base de la transplantation, notamment le caractère désintéressé du don.
Dans ce contexte, la proposition directive relative aux normes de qualité et de sécurité des organes humains destinés à la transplantation (document COM (2008) 818 final/E 4137) présentée par la Commission européenne en décembre 2008 et soumise à l’examen de la Commission des affaires européennes au titre de l’article 88-4 de la Constitution représente un exercice assez difficile, car elle s’insère dans un ordonnancement juridique déjà très développé avec, d’une part, des règles internationales à vocation universelle et, d’autre part, des règles nationales extrêmement bien établies, notamment parce qu’il s’agit d’une question sensible sur laquelle, sans d’ailleurs que l’on en identifie clairement les raisons, les différences d’approches sont fortes entre les Etats membres.
En outre, à l’échelon européen, une coopération existe déjà tant en raison des travaux du Conseil de l’Europe qu’à travers des structures de coopération mise en place entre certains Etats membres.
Néanmoins, telle qu’elle a été présentée et améliorée par les travaux du groupe santé publique préparatoire au Conseil et ceux du Parlement européen, qui ont débouché sur un texte d’équilibre, la proposition de directive réussit pleinement l’exercice et ne soulève pas d’objection pouvant s’opposer à son adoption.
I. UNE COMPÉTENCE ESSENTIELLEMENT NATIONALE ET POUR LAQUELLE UNE COOPÉRATION DIRECTE EST DÉJÀ ORGANISÉE, D’UNE PART, ENTRE CERTAINS ETATS ET, D’AUTRE PART, AU SEIN DU CONSEIL DE L’EUROPE
Les transplantations d’organes se développent, mais elles le font dans un contexte de pénurie permanente et récurrente.
En 2008, lors de présentation de la proposition de directive et du plan d’action, la Commission européenne a estimé à 50 000 personnes le nombre des patients en attente d’une transplantation d’organe.
Ce chiffre n’a pas diminué depuis. Il est évalué à 60 000 par le Parlement européen, dans un communiqué du 22 mars dernier.
Il en résulte d’abord d’importants délais d’attente, puisque le nombre de transplantations est de moins de 18 000 en Europe, soit une attente théorique de l’ordre de trois ans. Cette situation n’est pas en elle-même tolérable, car la vie des patients concernés est faite de tensions et d’appréhension.
Il en résulte aussi des décès. Des personnes meurent faute d’avoir pu bénéficier de la greffe dont elles ont besoin. La Commission européenne a ainsi évalué en 2008 à quelque douze décès par jour les conséquences de cette situation. Pour sa part, Alliance O a estimé en 2004 le taux de mortalité des personnes sur listes d’attente entre 5 % et 30 %, selon les pays et selon les types d’organes.
Le cas de quelques pays est, dramatiquement, éclairant.
S’agissant de la France, le dernier rapport de l’Agence de Biomédecine recense 424 décès de patients en attente de greffe pour 2008, dont 201 pour le rein, 107 pour le foie et 66 pour le cœur.
La situation est ailleurs comparable.
Pour ce qui concerne le Royaume-Uni, il y avait au 31 mars 2009, un total de 7 877 patients inscrits sur les listes de greffe actives et 2 385 patients étaient sur les listes de greffe temporairement suspendues, soit une augmentation de 3 % et 14 % respectivement sur les chiffres correspondants à la fin de l'année précédente. 448 patients sont morts en 2008-2009 en attente d’une greffe.
Pour ce qui est des temps d’attente, on enregistrait, en Italie, au 31 décembre 2008, un délai de plus de trois ans pour la greffe du pancréas, de deux ans pour celle du poumon, de trois ans pour le rein, ainsi que de deux ans pour le foie et le coeur.
La transplantation d’organes met en jeu les ressorts et les convictions les plus intimes de peuples. Elle concerne l’ultime question, celle de la mort, et de la vie, et interroge chacun sur ses relations avec son corps. Elle est donc très sensible et ne fait pas l’objet de réponses similaires.
L’enquête spéciale Eurobaromètre publiée en 2007 intitulée « Les Européens et le don d’organes » fait ainsi apparaître de nombreuses différences entre les pays.
En premier lieu, le don et la transplantation d’organes ne sont pas un sujet que l’on évoque toujours dans les discussions du cercle familial, dans l’intimité.
S’il a déjà été évoqué dans 41 % des familles européennes en moyenne, on constate de fortes divergences entre les douze Etats membres les plus récents, où l’on se situe entre 16 % (Roumanie) (puis 19 % en République tchèque et 22 % en Bulgarie) et 30 % (Slovaquie), et les autres, avec un minimum de 39 % pour la Grèce et de 75 % pour les Pays-Bas, suivis par la Suède (68 %) et le Danemark (58 %).
Avec 47 % des foyers ayant déjà évoqué la question, la France est au quatrième rang.
Dans l’ensemble, ce sont les femmes, les actifs d’âge intermédiaires, entre 25 et 54 ans, et les personnes dont le niveau professionnel est élevé qui en parlent davantage que les autres.
En deuxième lieu, il n’y a pas non plus d’homogénéité européenne sur le don de ses propres organes.
Si une majorité d’Européens se sont déclarés prêts le faire, s’agissant du don après la mort, à raison de 56 %, on constate là aussi des différences marquées entre les pays d’Europe du Nord où une très forte majorité est volontaire (81 % des Suédois, 73 % des Finlandais et des Belges, 69 % des Néerlandais et des Danois), ainsi que de Malte (75 %), et à l’exception de la Slovénie (63 % d’avis favorables) et de l’Estonie (58 %), des réticences dans les pays d’Europe centrale et orientale, notamment en Roumanie (27 % seulement de personnes prêtes à donner post mortem), ainsi qu’en Autriche (33 %) et en Italie (45 %).
Avec 67 %, la France se trouve en situation intermédiaire.
A l’exception des plus de 55 ans, dont 49 % seulement est favorable au prélèvement de ses propres organes après la mort, il n’y a pas de différences marquées entre le sexe et l’âge, sur cette question.
En revanche, l’éducation constitue un facteur de clivage important : les personnes dont le niveau d’étude est moins élevé sont dans l’ensemble plus réticentes que les autres au don d’organe.
Le fait d’avoir évoqué la question en famille n’est pas neutre. C’est même un facteur favorable pour que la perception du don soit positive.
En troisième lieu, on retrouve dans l’ensemble la même approche sur le don des organes d’un proche parent après son décès. Ce sont les pays d’Europe du Nord, Suède avec 74 % d’opinions favorables, puis Finlande avec 73 % et Pays-Bas qui marquent le plus d’allant, et les plus réticents sont la Roumanie (32 % d’opinions favorables) et l’Autriche (35 %).
Avec 61 %, la France se trouve également en position intermédiaire.
En quatrième et dernier lieu, même si les opinions des peuples sont beaucoup plus proches, il n’y pas non plus de véritable consensus des Européens sur le principe de l’utilisation de la carte de donneur d’organe.
Si 81 % des Européens sont favorables à cette carte pour faciliter l’identification des personnes disposées à faire un don d’organe après leur mort, contre 19 % qui y sont opposées, on observe que cette majorité n’atteint pas les deux tiers en Roumanie, où la proportion de « oui » n’est que de 49 %, ainsi qu’en Républiquen tchèque (60 % de oui), en Grèce (64 %), de même qu’en Slovaquie et en Lettonie (65 %).
Comme précédemment, c’est en Suède, ainsi qu’à Malte, que la carte recueille le plus grand assentiment (95 %) et la France est dans une situation intermédiaire (87 %).
Cette hétérogénéité de l’approche selon les peuples se constate également à l’intérieur des Etats. Au Royaume-Uni, les taux de prélèvement ne sont pas les mêmes en Angleterre, en Ecosse, en Irlande du Nord et au Pays de Galles à raison de 14,1 pour un million d’habitants en Ecosse, 12,2 en Irlande du Nord, 15,3 en Angleterre et 12,2 au Pays de Galles.
La principale différence entre les Etats membres concerne le consentement au don d’organes.
Certains pays appliquent la règle du consentement explicite. Un organe n’est prélevé que si le donneur a donné explicitement, de son vivant, son consentement à des prélèvements d’organes post mortem.
C’est le principe adopté par le Danemark, les Pays-Bas, le Royaume-Uni, l’Irlande et l’Allemagne.
En revanche, d’autres pays, dont la France, ont retenu la règle du consentement présumé, suivant laquelle le prélèvement est envisagé dès lors que le donneur n’a pas exprimé de refus de son vivant. C’est le cas, en plus de notre pays, de l’Autriche, de la Belgique, de l’Espagne, de la Finlande, de la Grèce, de l’Italie, du Luxembourg, du Portugal et de la Suède.
Cette différence d’approche est d’autant plus essentielle qu’elle porte sur un sujet sensible.
En pratique néanmoins, les procédures sont assez voisines, selon l’Agence de la Biomédecine, car l'ensemble des pays pratique l’entretien avec la famille pour prendre connaissance des volontés du défunt, le plus souvent très peu exprimées de son vivant. En outre, en cas de décès à l’étranger, c’est la règle de l’Etat d’origine du défunt qui s’applique.
En France, les refus des personnes qui manifestent leur refus sont enregistrés dans le registre national du refus (RNR). Celui-ci comptait 74 698 oppositions valides au 31 décembre 2008. 71 refus ont été identifiés lors de son interrogation depuis 1998, dont l’essentiel porte sur les tissus (48 refus de prélèvements) et le reste sur les organes (7 refus), sur les prélèvements à but scientifique (10 refus) et l’autopsie médicale (6 refus).
Au cours de l’année 2008, 4 012 inscriptions ont été validées et 11 refus ont été identifiés, dont 2 relatifs à des prélèvements à but thérapeutique.
La situation des différents pays européens en matière de greffe est très contrastée. Le total du nombre des dons et des greffes est très inégalement réparti.
S’agissant des dons, le volume 14 (no 1) précité de la lettre d’information Newsletter transplant fait apparaître que 8 959 donneurs décédés ont été recensés dans les vingt-sept Etats membres de l’Union européenne en 2008.
Quelques Etats regroupent la majeure partie des donneurs : la France avec 1 610, l’Espagne, avec 1 577, l’Allemagne à raison de 1 199 et l’Italie avec 1 201.
La carte suivante montre que ces données sont également très différentes selon les pays, rapportées au million d’habitants, allant de 34,2 donneurs décédés par million d’habitants en Espagne à 1,1 en Bulgarie.
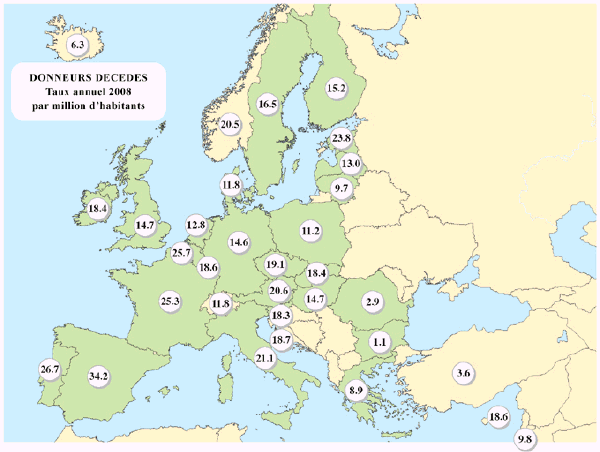
Sous une forme graphique, ces mêmes éléments sont repris par la Commission européenne.
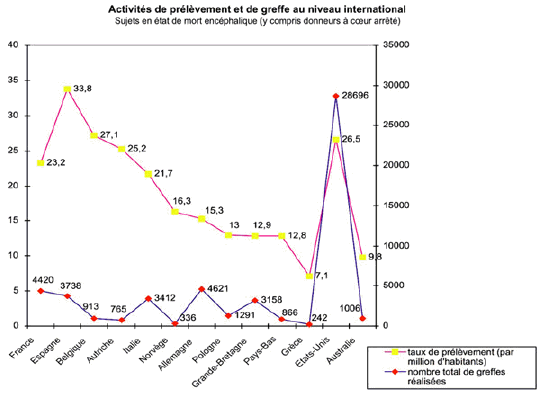
Source : Commission européenne.
Pour ce qui concerne les greffes, selon les éléments également publiés dans ce même volume de la lettre d’information Newsletter transplant, un peu plus de 27 800 greffes ont été réalisées dans l’Union européenne en 2008.
L’essentiel consiste en des greffes de rein (17 198), puis de foie (6 551), de cœur (2 011) et poumons (1 293) et, enfin, de pancréas (756).
Pour les plus nombreuses, les greffes de rein, l’essentiel est réalisé en France (2 885), puis en Allemagne (2 753), au Royaume-Uni (2 302), en Espagne (2 229), en Italie (1 656).
La répartition est inégale selon les Etats. La carte suivante, publiée dans le même fascicule, montre les écarts entre les greffes rénales rapportées au million d’habitants.
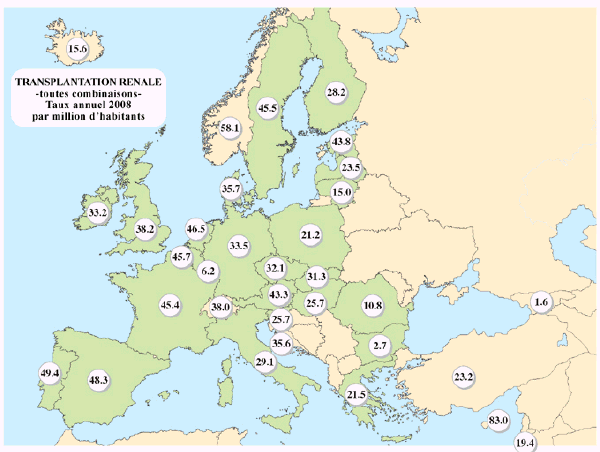
Le taux varie de 49,4 par million d’habitants au Portugal et 48,3 en Espagne à 6,2 au Luxembourg (les greffes se font dans les pays voisins) et 2,7 en Bulgarie. Avec 45,4 greffes rénales par million d’habitants, la France se situe dans le groupe de tête, de même que la Belgique, les Pays-Bas, la Suède, ainsi que l’Autriche et l’Estonie.
En France, comme toutes les thérapeutiques utilisant des éléments du corps humain autres que le sang (organes, tissus, cellules et gamètes), la greffe d’organe relève des compétences de l’Agence de la biomédecine, créée par la loi en 2004, et qui a succédé à l’Etablissement français des greffes.
En effet, celle-ci :
– gère la liste nationale des personnes en attente de greffe, ainsi que le registre national de prélèvement ;
– établit les règles de répartition des organes ;
– assure la répartition des prélèvements d’organes, ainsi que l’attribution et la répartition des greffons ;
– organise les travaux des comités d’experts autorisant le prélèvement sur donneur vivant ;
– suit l’état de santé des donneurs vivants ;
– développe, enfin, l’information sur le don, le prélèvement et la greffe, et assure la promotion du don.
L’Agence a conclu avec ses autorités de tutelle, le ministère de la santé et le ministère du budget, un contrat de performance 2007-2010, qui prévoit notamment parmi ses neuf orientations stratégiques la poursuite de l’amélioration de l’accès à la greffe et la contribution à la réflexion éthique, ainsi qu’à la diffusion et au respect des principes éthiques dans les activités relevant de son champ de compétence.
En 2008, 4 620 patients ont bénéficié d’une greffe, dont 232 à partir de donneurs vivants.
Le premier organe greffé est le rein, à raison de 2 937 dont 222 à partir de donneur vivant, puis viennent ensuite le foie (1 011, dont 10 provenant de donneurs vivants), le cœur (360), les poumons (196), le pancréas (84), l’ensemble cœur et poumons (19), et l’intestin (13).
La pénurie est particulièrement sensible puisque :
– 13 698 malades étaient en attente d’une greffe à la fin de 2008, dont 10 180 en attente d’une greffe de rein
– et surtout, 424 décès de patients en attente d’une greffe ont été enregistrés en 2008, dont 201 pour le rein, 107 pour le foie et 66 pour le cœur.
Pour ce qui concerne les prélèvements sur personnes décédées, 1 563, personnes en état de mort encéphalique, soit 24,6 par million d’habitants, et 47 personnes décédées après arrêt cardiaque ont fait l’objet d’un prélèvement en 2008.
Le pourcentage d’opposition a été de 30,7 % des personnes recensées.
En matière de dons d’organes, l’Espagne a connu un développement spectaculaire, puisque l’on est passé de 14 dons par million d’habitants en 1989 à 35,1 en 2005. L’évolution s’est faite en une décennie, puisque ce niveau a été atteint en fait dès 2000.
Ce succès est à l’origine des réflexions et travaux sur le « modèle espagnol », dont plusieurs pays, notamment l’Italie, l’Australie, le Brésil, ainsi que les Etats-Unis, se sont inspirés.
Sa portée est renforcée par la capacité de l’Organización nacional de trasplantes (ONT) a réaliser parfois des record d’activité et de coordination simultanée de plusieurs greffes.
Les commentaires sur la réussite de l’Espagne mettent l’accent sur le renforcement de la détection des donneurs potentiels, l’importance de la communication, la formation des équipes, notamment pour le dialogue avec les familles, dont l’avis est en pratique sollicité même si le consentement du défunt est présumé, le rôle clef des coordinateurs de transplantation implantés dans les hôpitaux ainsi que sur l’utilisation des greffes dites limites, qui se traduit notamment par l’augmentation de l’âge moyen des donneurs, passé de 34 à 47 ans entre 1992 et 2000.
En outre, sans que l’on sache si cela influe ou non sur la décision des familles, on autorise la prise en charge des frais d’obsèques ou, pour les étrangers, les frais de rapatriement du corps, ce qui constitue « une sorte de compensation », selon les termes des Drs David Rodriguez-Arias Vailhen et Manuel Wolf dans leur article « la transplantation d’organes en Espagne et en France : éléments pour une compréhension du modèle espagnol ».
Sur le fond sinon, les mêmes principes de base sont appliqués en France et en Espagne : consentement présumé, séparation entre les équipes de prélèvement et les équipes de greffe ; anonymat et gratuité du don.
B. Une intervention communautaire prévue par le traité, mais récente, d’ampleur assez réduite et qui doit trouver sa place entre des coopérations directes entre Etats et une action très positive du Conseil de l’Europe
Sur le fond, la compétence européenne en matière de transplantation d’organes est assez récente.
Elle n’a pas été prévue par le traité de Maastricht, en 1992, qui, le premier, a donné à la Communauté une compétence en matière de santé. Il s’agissait alors d’une compétence d’encouragement à la coopération des Etats membres et d’appui de leur action, exclusive de toute harmonisation législative et règlementaire et ainsi limitée pour l’essentiel à des recommandations.
En effet, elle a été introduite cinq ans plus tard, en 1997, par le traité d’Amsterdam, qui a inséré dans le traité de Rome les actuelles dispositions, lesquelles ont été reprises dans l’actuel article 168 du traité sur le fonctionnement de l’Union européenne.
Celui-ci prévoit que pour atteindre les objectifs prévus en matière de santé publique, le Parlement européen et le Conseil peuvent adopter des mesures fixant des normes élevées de qualité et de sécurité des organes, ainsi d’ailleurs que sur les substances d'origine humaine, le sang et les dérivés du sang, et que ces mesures ne peuvent empêcher un Etat membre de maintenir ou d'établir des mesures de protection plus strictes.
Il précise également que ces dispositions ne portent pas atteinte aux dispositions nationales en matière de dons d’organes.
La compétence de l’Union est donc en la matière une compétence complémentaire à celle des Etats membres, et strictement limitée aux normes et à la fixation de normes minimales. En particulier, les questions éthiques ne ressortissent pas à la compétence communautaire.
Par ailleurs, l’Union européenne connaît également de la question des transplantations d’organes dans le cadre des programmes de recherche. Plusieurs projets liés au don et à la transplantation d’organes sont ainsi en cours.
2. Des coopérations entre Etats membres directes, structurées, multilatérales et organisées depuis longtemps
En matière de dons et transplantations d’organes, certains Etats européens ont déjà organisés entre eux des coopérations, sur une base multilatérale d’ailleurs, le plus souvent.
Eurotransplant a été créée en 1968 à Leyde, aux Pays-Bas, et regroupe les laboratoires d’histocompatibilité et les coordinateurs des Etats suivants : l’Allemagne, l’Autriche, la Belgique, le Luxembourg, les Pays-Bas et la Slovénie.
L’objectif est d’éviter la perte des organes disponibles grâce à un champ territorial plus large. L’organisation repose sur le principe de la centralisation des données médicales, sérologiques et administratives à Leyde, données à partir desquelles se fait la sélection du meilleur receveur possible pour un organe donné.
Scandiatransplant regroupe le Danemark, la Finlande et la Suède, ainsi que, hors de l’Union européenne, la Norvège et l’Islande. Il a été fondé en 1969 à Aarhus, au Danemark. Il repose sur le même principe d’une base de données commune et de la gestion des échanges transfrontaliers d’organes.
UK transplant, qui s’appelle depuis 2008 le Directorate of Organ Donation & Transplantation, exerce ses compétences sur le Royaume-Uni et la République d’Irlande.
S’agissant de la France, notre pays dispose, pour la transplantation hépatique, d’un accord entre Swisstransplant et l’Agence de biomédecine (initialement, cet accord a été conclu avec l’Etablissement français des greffes, organisme prédécesseur de l’Agence) lequel prévoit que les équipes chirurgicales suisses ont accès au territoire français pour les grandes urgences et que tout greffon suisse pour qui un receveur compatible ne peut pas être identifié est offert prioritairement à la France.
Il faut rappeler la coopération menée dans le cadre du projet Alliance O pendant trois années entre les Agences en charge de la greffe d’organes de sept pays (Allemagne, Espagne, France, Hongrie, Italie, Portugal et Royaume-Uni). Ce projet a été piloté par l’Agence de la biomédecine.
Egalement co-financé par la Commission Européenne à hauteur de deux millions d’euros pour mettre en commun leur savoir-faire et leurs pratiques et faire avancer leur réflexion dans le domaine de la greffe, ce projet a eu pour objet de coordonner les programmes nationaux et régionaux de chacun de ces pays autour de six axes de travail :
– l’augmentation du nombre de donneurs (décédés et vivants) ;
– l’amélioration de l’équité et de l’efficacité des règles de répartition ;
– l’amélioration de la qualité de la greffe d’organes ;
– l’amélioration des méthodes d’évaluation de l’activité de prélèvement et de greffe ;
– l’amélioration de la coordination en recherche fondamentale ;
– l’analyse comparative des aspects éthiques et légaux du prélèvement et de la greffe.
Les travaux conduits dans ce cadre ont permis un partage d’expertise, qui a débouché sur le constat d’importantes différences pratiques entre les Etats et sur la nécessité d’améliorer l’organisation et les pratiques de chaque pays et de renforcer les collaborations.
Ils se sont conclus par des recommandations, regroupées dans un livre blanc et publiées en octobre 2007, avec l’objectif de réduire la pénurie des greffons.
Celles-ci sont les suivantes :
– l’augmentation du nombre de donneurs, avec notamment des éléments méthodologiques pour mieux mobiliser et utiliser les différentes possibilités (développement des techniques permettant d’utiliser les donneurs limites, etc) ;
– l’amélioration de l’équité et de l’efficacité des règles de répartition des greffons ;
– l’amélioration de la qualité et de la sécurité de la greffe d’organes : quels tests pour sélectionner les donneurs ? Quelles procédures de qualité dans les différentes phases de la greffe, du don jusqu’au suivi du patient après l’intervention ?
– l’amélioration des méthodes d’évaluation de l’activité de prélèvement et de greffe, avec notamment la mise au point de systèmes de biovigilance ;
– l’amélioration de la coordination en recherche fondamentale sur le prélèvement et la greffe d’organes ;
– des recommandations, enfin, sur l’analyse comparative éthique, le conclusions insistant sur le fait qu’il n’est pas éthique que tous les donneurs potentiels ne soient pas recensés et sur la nécessité de s’opposer à une rémunération du donneur ou de ses proches dans le cas d’un don post-mortem.
4. Les instruments juridiques et interventions du Conseil de l’Europe, notamment dans la lutte contre le trafic international d’organes
Une coopération entre les Etats européens, dans un cadre cependant plus large que celui de l’Union européenne, a été engagée sur l’initiative du Conseil de l’Europe.
Conformément à l’article 1er de son statut, suivant lequel « le but du Conseil de l'Europe est de réaliser une union plus étroite entre ses membres afin de sauvegarder et de promouvoir les idéaux et les principes qui sont leur patrimoine commun et de favoriser leur progrès économique et social », celui-ci a pour objectif de protéger la dignité et les droits fondamentaux de la personne vis-à-vis des applications de la biologie et de la médecine.
Deux instruments juridiques sont ainsi intervenus.
Le premier est la convention, dite d’Oviedo, pour la protection des droits de l'homme et de la dignité de l'être humain à l'égard des applications de la biologie et de la médecine (également appelée Convention sur les droits de l'homme et la biomédecine), du 4 avril 1997. Elle fixe principes fondamentaux applicables à la médecine quotidienne, ainsi que ceux applicables aux nouvelles technologies dans le domaine de la biologie humaine et de la médecine.
Le second lui est complémentaire. Il s’agit du Protocole additionnel à cette convention, relatif à la transplantation d'organes et de tissus d'origine humaine, du 24 janvier 2002. C’est, selon les informations communiquées, le seul instrument juridique actuellement contraignant en la matière.
Comme toutes questions de bioéthique, le sujet est étroitement suivi par le Conseil de l’Europe, notamment au sein du Comité directeur pour la bioéthique (CDBI).
Dans le cadre de la Pharmacopée, a également été élaboré un Guide sur la sécurité et l’assurance de qualité de la transplantation d’organes, de tissus et de cellules. Celui-ci est régulièrement révisé.
Pour ce qui concerne la lutte contre le trafic international d’organes, une Etude conjointe du Conseil de l’Europe et des Nations unies sur le trafic d’organes, de tissus et de cellules et la traite des Etres humains aux fins de prélèvement d’organes vient d’être réalisée. Sur la base de ses recommandations, le Comité des ministres a demandé que soit étudié un instrument définissant ce trafic international et permettant de prévoir les sanctions pénales appropriées.
Pour sa part, l’Assemblée parlementaire du Conseil de l’Europe se saisit régulièrement de la question des transplantations d’organes.
Sur le rapport de Mme Vermot-Mangold (Suisse), elle a ainsi adopté la recommandation 1611 (2003) sur la lutte contre le trafic d’organes en Europe.
Actuellement, des travaux sont en cours sur ce même type de trafic au Kossovo, M. Dick Marty (Suisse) étant rapporteur.
II. LA PROPOSITION DE DIRECTIVE SUR LES TRANSPLANTATIONS D’ORGANES : UNE TEXTE D’ÉQUILIBRE, UTILE ET RESPECTUEUX DU PRINCIPE DE SUBSIDIARITÉ
Lors de leur réunion du 7 juillet 2008, à Paris, dans le cadre de la « petite COSAC », les présidents des organes spécialisés dans les affaires communautaires ont fait droit à la suggestion de la France d’inscrire dans la liste des textes devant faire l’objet d’un test concerté de subsidiarité, la future proposition de directive du Parlement européen et du Conseil relative aux normes de qualité et de sécurité des organes humains destinés à la transplantation.
Cette décision a ensuite été confirmée par les conclusions de la XLe COSAC, qui s’est tenue les 3 et 4 novembre à Paris.
Le mardi 9 décembre suivant, le secrétariat de la COSAC a communiqué les textes anglais et français de la proposition, présentée la veille par la Commission européenne.
Le lendemain, 10 décembre, il a informé par e-mail les parlements nationaux que l’ensemble des traductions étant disponibles, le délai de 8 semaines pour effectuer l’examen commençait à courir et que la date limite pour la transmission des avis était le 6 février 2009.
Le calendrier a été court, puisque la date limite a été fixée au 6 février 2009.
On peut le regretter car les dons, obtentions et transplantations d’organes concernent, en effet, la vie et la mort, la relation de l’homme avec son corps, ses liens à autrui. Ils mettent ainsi en jeu le plus profond des convictions éthiques, philosophiques, ainsi que religieuses, de chacun.
L’objectif d’un test de subsidiarité est de s’assurer que les principes de subsidiarité et de proportionnalité sont bien respectés et que, dans un domaine de compétence partagée, le niveau communautaire n’empiète pas sur les prérogatives des Etats membres.
Il s’agit de répondre à deux questions :
– la Communauté européenne est-elle fondée à intervenir et à ne pas laisser les Etats membres agir seuls en la matière ?
– si tel est le cas, le principe de proportionnalité est-il respecté ? Le dispositif proposé n’excède-t-il pas ce qui relève du niveau communautaire ?
Ces questions ne se sont pas encore posées pour le domaine précis des organes d’origine humaine, en l’absence de texte communautaire applicable.
Ce sujet n’est cependant pas totalement étranger à l’Europe, puisque de nombreux programmes de recherche ont fait l’objet de cofinancements communautaires.
Pour ce qui concerne le principe de subsidiarité, il faut d’abord observer que l’article 152 du traité instituant la Communauté européenne, applicable au moment du test de subsidiarité, qui y a été introduit par le traité d’Amsterdam, fournit une base juridique claire à une intervention communautaire en la matière :
– le a) du point 4. permet l’adoption de « mesures fixant des normes élevées de qualité et de sécurité des organes et substances d’origine humaine », ainsi que du sang et des dérivés du sang, sans que ces mesures empêchent « un Etat membre de maintenir ou d’établir des mesures de protection plus strictes » ;
– le 5. donne des précisions sur l’articulation des compétences de la Communauté et des Etats membres : « l’action de la Communauté dans le domaine de la santé publique respecte pleinement les responsabilités des Etats membres en matière d’organisation et de fourniture de services de santé et de soins médicaux. En particulier, les mesures ne portent pas atteinte aux dispositions nationales relatives aux dons d’organes et de sang ou à leur utilisation à des fins médicales. »
Le traité de Lisbonne n’apporte en la matière aucun changement de fond.
C’est sur cette même base juridique que sont d’ailleurs déjà intervenus plusieurs textes régissant le sang et les composants sanguins (directives 2002/98/CE, 2004/33/CE, 2005/61/CE et 2005/62/CE), ainsi que les cellules et les tissus humains (directives 2004/23/CE, 2006/17/CE et 2006/86/CE).
La proposition de directive apparaît donc comme un complément des textes déjà intervenus en matière de substances et organes d’origine humaine.
Au regard du principe de subsidiarité toujours, le dispositif prévu appelle cinq séries d’observations.
En premier lieu, les différences actuelles de niveau entre les Etats membres en matière d’organes, tant en matière de nombre d’obtention que de sécurité et de qualité sanitaires, peuvent effectivement justifier une intervention communautaire, au regard de l’objectif du haut niveau de protection de la santé humaine fixé par le traité. Néanmoins, sauf cas des pays qui coopèrent entre eux dans des cadres spécifiques comme Eurotransplant et Scandiatransplant, les échanges d’organes transfrontaliers sont très faibles. Pour ce qui concerne la France, en 2007, le rapport de l’Agence de biomédecine mentionne l’importation de 4 greffons (4 cœurs) et l’exportation de 21 greffons (3 reins, 9 foies, 7 cœurs, 2 poumons). Cette même année, 1.562 donneurs décédés ont effectivement donné lieu à prélèvement et 4.666 greffes d’organes, dont 253 à partir de donneurs vivants, sont intervenues. Les transferts de greffons d’un pays à l’autre sont marginaux car le délai doit être bref entre le prélèvement et la transplantation : le délai maximum va de 6 à 20 heures selon l’organe et le taux de survie après la greffe est d’autant plus élevé que ce délai entre les deux phases est réduit, en l’état actuel des techniques utilisées.
En deuxième lieu, la proposition ne contient pas la totalité des actions prévues par la Commission européenne en la matière.
Une partie des mesures proposées relève, en effet, du plan d’action sur le don et la transplantation d’organes (2009-2015), présenté en même temps que la proposition de directive, dans le cadre d’une communication spécifique de la Commission européenne (document COM [2008] 819 final).
Ce plan s’inscrit dans le cadre de la compétence communautaire d’encouragement à la coopération entre les Etats membres et d’appui à leurs actions, prévue au 2 de l’article 152 précité du traité.
Dans ces circonstances, la proposition de directive s’en tient à l’essentiel, en :
– imposant aux Etats membres de disposer chacun d’un programme national de qualité couvrant toutes les étapes de la chaîne, du don jusqu’à la transplantation ou à l’élimination, ainsi que d’une autorité de contrôle de l’ensemble de ces activités, ainsi qu’en leur demandant de veiller à ce que les organismes d’obtention (c'est-à-dire les établissements de prélèvements d’organes) répondent aux règles qu’elle prévoit, notamment la supervision d’un médecin pour la sélection des donneurs et des installations spécifiques répondant à des normes précises pour éviter le risque bactérien ;
– prévoyant l’obligation de caractériser les organes et les donneurs, avant toute transplantation, grâce à la collecte d’informations et de données, afin d’éviter la transmission de pathologies du donneur au receveur ;
– donnant des règles précises pour les centres de transplantation, notamment un régime d’autorisation, désignation, agrément ou licence, et des obligations sanitaires ;
– imposant une traçabilité du donneur au receveur, et inversement ;
– demandant un système de notification des incidents et réactions indésirables, avec interconnexion au système de vigilance prévu par la directive 2004/23/CE concernant les tissus et cellules ;
– prévoyant des règles minimales de protection du donneur et du receveur, notamment les principes régissant le don d’organes (caractère volontaire, absence de rémunération, caractère non lucratif de l’activité d’obtention d’organes), de même que des règles pour l’information du donneur vivant ;
– organisant l’échange d’informations entre autorités compétentes des Etats membres ;
– fixant le cadre des échanges avec les pays tiers, notamment en imposant une traçabilité pour éviter les trafics.
En outre, la proposition de directive confirme la possibilité de coopérations entre certains Etats membres, ce qui permet aux pays concernés de conserver les organisations en fonctionnement : Scandiatransplant (Danemark, Finlande et Suède, ainsi que, hors de l'Union européenne, Norvège) et Eurostransplant (Allemagne, Autriche, Belgique, Luxembourg, Pays-Bas, Slovénie), ainsi que UK transplant (Royaume-Uni et Irlande).
En troisième lieu, la proposition de directive respecte bien les attributions des Etats membres sur la question du consentement et des autorisations préalables à l’obtention d’un organe, qui relèvent pleinement de leurs compétences comme, d’une manière générale, les questions de bioéthique. Il est explicitement inscrit que « l’obtention ne peut avoir lieu que si toutes les exigences en matière de consentement ou d’autorisation préalable en vigueur dans l’Etat membre concerné ont été remplies ».
Outre le strict respect du principe de subsidiarité, une telle précision est essentielle car la définition du décès et les modalités de son constat ne sont pas les mêmes dans les différents Etats membres. Cet élément fait d’ailleurs obstacle à la mise en place d’une carte européenne de donneur, en dépit de l’allant que suscite dans un premier élan une telle idée.
En quatrième lieu, même si la lettre du traité ne mentionne que les normes de « sécurité et de qualité des organes » et non les transplantations, il convient de ne pas soulever d’objection sur ce point, dans la mesure où le respect de la continuité de la chaîne qui va de l’obtention à l’implantation doit primer sur toute autre considération. Le principe de sécurité sanitaire s’impose. La future directive doit bien couvrir, comme le demande la Commission européenne, le prélèvement comme l’implantation d’organes.
En cinquième lieu, enfin, compte tenu de la répartition des mesures entre le plan d’action et la proposition de directive, cette dernière fixe un cadre administratif et sanitaire incontestable et d’autant plus acceptable qu’il ne pose, en outre, pas de problème d’adaptation pour notre pays, selon les informations communiquées. Le dispositif proposé présente, en effet, l’avantage d’être suffisamment flexible.
En ce qui concerne le respect du principe de proportionnalité, le dispositif initialement proposé par la Commission européenne n’a pas, non plus, appelé de réserve, même s’il recelait une incertitude sur un point, celui du statut de la liste de caractérisation des organes figurant dans le formulaire qui sera annexé à la future directive, et plus précisément de la liste des données, notamment biologiques, exigées pour permettre au centre de transplantation d’établir de manière adéquate les risques et avantages de l’opération envisagée.
Sur ce point, comme d’une manière générale, il doit être clair que l’adoption du cadre communautaire ne doit pas entraîner, même de manière imprévue, quelque régression que ce soit du niveau des transplantations dans un Etat membre donné. Il ne saurait être question que les niveaux d’excellence atteints par certains pays dans certains domaines puissent être remis en cause.
En l’état, la proposition de directive n’a pas appelé, par conséquent, de réserve susceptible de justifier son réexamen par la Commission européenne, au regard des principes de subsidiarité et de proportionnalité.
Dans ces circonstances, conformément à la proposition des rapporteurs, la Commission, au cours de sa réunion du 28 janvier 2009, a adopté, au regard de la subsidiarité et de la proportionnalité, les conclusions suivantes sur la proposition de directive du Parlement européen et du Conseil relative aux normes de qualité et de sécurité des organes humains destinés à la transplantation (COM [2008] 818 final) :
« La Commission chargée des affaires européennes considère que la proposition de directive n’est pas, à ce stade et en l’état des informations dont elle a pu disposer, contraire aux principes de subsidiarité et de proportionnalité. »
Pour sa part, le Sénat français a partagé l’avis de l’Assemblée, et considéré qu’il n’y avait pas atteinte au principe de subsidiarité ni de proportionnalité.
Présenté dans le cadre de la XLIe COSAC, organisée du 10 au 12 mai 2009 à Prague, le rapport sur les résultats du contrôle de subsidiarité au sujet de la proposition de directive précise que l’immense majorité des assemblées parlementaires des Etats membres qui ont participé au test n’ont pas constaté de violation du principe de subsidiarité.
D’une manière précise, vingt-sept assemblées de vingt Etats membres ont répondu dans les délais.
Ensuite, quatre assemblées supplémentaires ont communiqué leur avis.
Au total, trente-et-une chambres de vingt trois Etats membres se sont prononcées.
Une seule chambre parmi les vingt-sept ayant répondu dans les délais, et donc participant au contrôle, a constaté une violation du principe de subsidiarité : le Bundesrat d’Autriche, dont la commission des affaires européennes a voté le 3 février 2009 une déclaration à l’adresse de la Commission européenne.
Ensuite, hors délais, une autre chambre a également eu un avis négatif : le Bundesrat allemand.
Néanmoins, de nombreuses assemblées ont considéré que la Commission européenne n’avait pas suffisamment développé les motifs concluant au principe de subsidiarité.
Ont ainsi demandé des éclaircissements et des informations avant de pouvoir prendre une décision définitive le Bundestag allemand, la Chambre des Communes du Royaume-Uni et le Sénat italien.
Hors délais, cette même position a été prise par les Pays-Bas.
Par ailleurs, la Chambre des Députés du Luxembourg a soulevé la question de l’adéquation entre la proposition de directive et les initiatives du Conseil de l’Europe.
Parmi les assemblées parlementaires qui ont néanmoins rendu un avis positif, un grand nombre d’entre elles a manifesté son regret quant à une subsidiarité insuffisamment motivée, notamment le Sénat français, le parlement irlandais, les deux chambres du Royaume-Uni, les deux chambres du Parlement italien et l’assemblée slovène.
Au total, la réponse des assemblées parlementaire a donc été qu’il n’y avait pas atteinte au principe de subsidiarité, mais sans que ce soit toujours les motifs invoqués en ce sens par la Commission européenne qui aient été de nature à emporter leur conviction.
Ainsi que leurs interlocuteurs l’ont précisé aux rapporteurs, la proposition de la Commission européenne n’a pas visé à créer ex nihilo un cadre communautaire relatif à la qualité et à la sécurité des organes, mais s’inscrit pleinement dans la perspective tracée, d’une part, par les travaux du Conseil de l’Europe et, d’autre part, par ceux réalisés dans le cadre du projet Alliance O qui s’est achevé en 2007.
Il n’introduit ni rupture intellectuelle, ni rupture scientifique, mais s’inscrit au contraire dans le cadre des travaux antérieurs menés en coopération.
La proposition de directive ne concerne que les seuls organes humains. Les autres « produits » d’origine humaine font déjà l’objet d’un cadre communautaire :
– la directive 2002/98/CE du 27 janvier 2003 a établi des normes de qualité et de sécurité pour la collecte, le contrôle, la transformation, la conservation et la distribution du sang humain, et des composants sanguins ;
– la directive 2004/23/CE du 31 mars 2004 relative à l'établissement de normes de qualité et de sécurité pour le don, l'obtention, le contrôle, la transformation, la conservation, le stockage et la distribution des tissus et cellules humains a fixé les règles en la matière.
Elle concerne la transplantation à des fins thérapeutiques, ainsi qu’à des fins de recherche (la recherche sur les organes sans transplantation est cependant exclue).
c) La reprise du triptyque de base : autorité nationale de contrôle, contrôle des établissements de prélèvement, autorisation des centres de transplantation
Sur le plan général, la proposition de directive prévoit que les Etats membres doivent respecter les principes de base d’une organisation efficace en matière de transplantation avec trois obligations :
– une autorité nationale compétente, telle que l’Agence de biomédecine en France, investie d’une mission générale d’organisation et de surveillance de l’activité de greffe ;
– un encadrement des organismes d’obtention, ou centres de prélèvement ;
– une autorisation des centres de transplantation.
L’objectif est de permettre d’appliquer effectivement les normes prévues de qualité et de sécurité.
d) Des dispositions relatives à la qualité et la sécurité des organes qui couvrent l’ensemble de la chaîne, du prélèvement jusqu’au suivi du bénéficiaire de la greffe comme du donneur vivant
Les règles relatives à la sécurité et à la qualité des organes constituent l’essentiel du dispositif de la future directive.
Elle reposent sur :
– un cadre de sécurité et de qualité (initialement, la Commission européenne avait souhaité un programme national) ;
– des règles sur l’obtention d’organes, sur la caractérisation des organes et des donneurs, sur le transport des organes et les centres de transplantation ;
– une obligation de traçabilité, dans le respect de l’obligation de confidentialité et de protection des données personnelles ;
– un dispositif de notification des incidents et des réactions indésirables graves, et une obligation de suivi du bénéficiaire de la greffe comme du donneur vivant ;
– une obligation de formation adéquate des personnels impliqués dans l’ensemble de la chaîne, allant du don jusqu’à la transplantation.
Pour les mesures qui relèvent de la comitologie, une nouvelle instance est créée, le comité sur la transplantation d’organes.
a) Un objectif partagé de sécurité et de qualité en faveur d’une convergence vers le haut des pratiques européennes
Le premier objectif, celui d’une amélioration de la qualité notamment des organes prélevés, et d’un renforcement de la sécurité des procédures et des greffes n’appelle pas d’observation particulière.
Les Etats membres ne sont pas actuellement tous dans des situations comparables et il est légitime que l’Union européenne vise à assurer une convergence dans le cadre d’une harmonisation vers le haut.
Plusieurs Etats membres sont indiqués comme dans l’attente de cette directive pour faire évoluer leur dispositif national, notamment en Europe centrale et orientale où comme on l’a vu, les transplantations sont moins courantes.
Le deuxième grand objectif visé par la Commission européenne est la réduction de la pénurie d’organes, avec deux éléments.
D’une part, des incitations au don sont prévues dans le cadre du plan d’action avec notamment des échanges d’informations entre les Etats membres et des campagnes de sensibilisation du public. Il s’agit de mettre fin au paradoxe suivant lequel 81 % des européens se disent favorables à la carte de donneur et seuls 12 % la possèdent.
D’autre part, la Commission européenne, de même d’ailleurs que le rapporteur du Parlement européen, M. Miroslav Mikolášik (PPE, Slovaquie), escomptent que la coopération entre les Etats, qui repose notamment sur les modalités d’échange d’informations prévues dans la future directive, permettra par une plus grande fluidité de mieux répondre aux besoins des citoyens européens. On peut néanmoins douter que la coopération et l’harmonisation, si elles créent les conditions d’un échange entre les Etats membres, puisse effectivement conduire à une augmentation de la disponibilité des organes.
Comme l’ont précisé aux rapporteurs plusieurs de leurs interlocuteurs, le contexte de pénurie générale des organes va persister et, malheureusement, ce n’est pas le partage de la pénurie qui engendre l’abondance.
Telle qu’elle est prévue, la proposition de directive permet d’envisager de lutter efficacement contre une partie du trafic international d’organes.
Elle impose, en effet, que tout échange d’organe soit supervisé par l’autorité nationale compétente, ave faculté de délégation à un organisme européen d’échange tels que ceux précités (Eurotransplant et Scandiatransplant notamment). Des accords peuvent être également avec les pays tiers. Comme précédemment indiqué, les greffes hépatiques font, pour la France, l’objet d’un accord avec la Suisse.
Sur le fond, ces autorisations et accords doivent prévoir la condition essentielle pour éviter tout trafic : la traçabilité de l’organe.
En outre, les normes de qualité et de sécurité doivent être équivalentes à celles prévues par la future directive.
Ce dispositif ne représente cependant que l’un des volets de cette lutte.
D’une part, celle-ci exige au-delà des textes plus généraux et impliquant un plus grand nombre d’Etats, comme le fait déjà le Conseil de l’Europe.
D’autre part, la dimension externe du trafic d’organe, à savoir le tourisme médical lié aux transplantations, ne doit pas être négligé.
Plusieurs organismes de transplantation et sociétés savantes ont ainsi adopté la déclaration dite d’Istanbul, rédigée en mai 2008 à l’initiative de la Société internationale de transplantation (TTS) et de la Société internationale de néphrologie par 150 représentants gouvernementaux et responsables médicaux et scientifiques, dont l’Agence de la biomédecine, sur le trafic d’organes et le tourisme de transplantation.
La proposition de directive ne contient pas la totalité des actions prévues par la Commission européenne en la matière.
Une partie des mesures proposées relève, en effet, du plan d’action sur le don et la transplantation d’organes (2009-2015), présenté en même temps que la proposition de directive, dans le cadre d’une communication spécifique de la Commission européenne (document COM [2008] 819 final).
Ce plan s’inscrit dans le cadre de la compétence communautaire d’encouragement à la coopération entre les Etats membres et d’appui à leurs actions, prévue au 2 de l’article 152 précité du traité.
Il a été bâti autour de 10 actions prioritaires avec, pour l’essentiel : la mise en place de coordinateurs de transplantation ; des cadres d’amélioration de la qualité concernant les dons d’organes (élément commun avec la proposition de directive) ; l’échange de bonnes pratiques sur les programmes de dons d’organes de donneurs vivants ; l’échange d’organes entre Etats membres pour les cas d’urgence et les patients difficiles à traiter ; des registres facilitant l’évaluation des résultats post-transplantation ; une méthodologie permettant de contribuer à créer, à terme, un système commun d’accréditation des programmes de don, d’obtention et de transplantation d’organes.
Ce plan a été favorablement accueilli par le Parlement européen, qui a adopté le rapport d’initiative de M. Andres Perello Rodrigues (S&D, Espagne).
1. Une absence d’interférence avec les compétences des Etats membres en matière de choix bioéthiques
L’examen des propositions de directive dont les sujets confinent à la bioéthique doit toujours faire l’objet d’un examen particulièrement attentif. Ces choix sont de la compétence des Etats membres et ne ressortissent pas à celle de l’Union européenne.
Ce sont en effet des choix sensibles, difficiles et délicats qui touchent à l’intimité et aux conceptions profondes des peuples. Ils sont directement liés à ses propres conceptions, philosophiques, morales ou religieuses, de l’homme, de la vie, de la mort, de la science, du corps, de l’interdit, de l’autorisé, de l’altruisme, du don, du gratuit, du commercial et du marchand. A terme, on peut souhaiter une convergence européenne, mais tel n’est pas encore le cas. Il convient d’en tenir compte.
Lors de l’examen de la proposition de directive sur les médicaments de thérapie innovante, la tentation de déborder du cadre initial de la proposition de la Commission européenne avait été présente.
Tel na pas été cette fois-ci le cas. Il faut donc rendre hommage à tous ceux qui ont participé aux travaux préparatoires, notamment aux membres du Parlement européen et à son rapporteur, M. Miroslav Mikolášik (PPE, Slovaquie).
Des idées aussi séduisantes que généreuses, mais très difficiles à mettre en place, ne sont donc pas proposées. Tel est par exemple le cas de la carte européenne de donneur d’organe, prévue par le rapport d’initiative du 1er avril 2008 sur les actions politiques au niveau de l'Union européenne concernant le don et la transplantation d'organes, adopté sur le rapport de M. Adamos Adamou (GUE/GVN, Chypre). Celle-ci ne pouvait déboucher sur un mécanisme simple, car, comme on l’a vu, faute d’unité de point de vue et de communauté de droit entre les Etats membres en matière de dons d’organes, cet instrument n’aurait pas pu avoir la même signification selon la nationalité ou l’Etat de résidence de son titulaire.
Il faut également rendre un hommage particulier à la Présidence espagnole qui a su, d’ailleurs forte de l’expertise de la médecine espagnole, trouver des propositions de compromis parfaitement équilibrées et adaptées.
Un important travail technique a été opéré pour parvenir à des positions communes notamment sur les définitions, le remplacement des programmes nationaux de qualité par un cadre de qualité et de sécurité et la définition des procédures.
Sur le plan bioéthique, le projet de compromis se limite ainsi, dans le respect du principe de subsidiarité, à apporter des précisions utiles sont ajoutées sur les notions clefs de consentement et de gratuité.
Sur celle de gratuité du don, est prévu que le désintéressement du donneur vivant ne fait pas obstacle à la compensation des dépenses qu’il engage et des pertes de revenu qu’il subit en raison du prélèvement. Pour éviter tout risque, les principes d’absence d’incitations financières et de bénéfice pour le donneur sont tout autant réaffirmés.
Sur le consentement, le texte fait clairement référence aux deux systèmes en vigueur dans les Etats membres : celui du consentement explicite et celui du consentement présumé.
Par rapport au texte initial de la proposition de directive, le texte de compromis comprend plusieurs apports qu’il convient de relever.
D’abord, conformément au modèle espagnol, le rôle essentiel, au niveau hospitalier, du coordinateur dans la réussite de la transplantation est affirmé.
Ensuite, est introduite une référence à l’analyse bénéfices/risques, selon la même démarche que pour le médicament, de la transplantation dans certains cas particulier. Il s’agit de permettre à l’équipe médicale de permettre la transplantation lorsque les avantages qu’elle peut procurer au patient sont plus importants que les risques éventuellement posés par l’absence de données de caractérisation sur certains éléments. Tel est notamment le cas lorsque la mort est certaine en l’absence de transplantation.
Enfin, des éléments sont ajoutés sur les compétences de la Commission européenne pour les actes d’exécution en matière d’échanges d’organes entre les Etats membres et les modalités de contrôles du Conseil et du Parlement européen. Les trois questions concernées sont la caractérisation du donneur et de l’organe, les procédures de transmission d’un Etat membre à l’autre et de rapport.
Pour la France, l’objectif de résorption des divergences actuelles de qualité et de sécurité ne devrait pas entraîner de bouleversement.
Selon les informations communiquées aux rapporteurs par l’Agence de Biomédecine, la France respecte déjà, pour l’essentiel, les dispositions prévues notamment en matière de traçabilité, de suivi des greffons et de système des autorisations, ainsi que d’organisation d’une autorité nationale compétente. Les centres de prélèvement font déjà, en effet, l’objet d’une certification et accréditation. Il convient alors uniquement d’achever la mise en place du mécanisme d’évaluation des résultats des équipes de greffe.
Par ailleurs, lors de la transposition, il conviendra de veiller à ce que les compétences de l’organisme national, l’Agence de biomédecine, respectent les obligations prévues en matière de transport des organes, ainsi que de formation des personnels, selon les informations communiquées.
b) Des dispositions qui donnent la souplesse demandée à l’annexe sur la caractérisation des organes et des donneurs
Lors de l’examen en janvier 2008 de la proposition de directive au titre du respect du principe de subsidiarité et de proportionnalité, la question du statut de la liste de caractérisation des organes figurant dans le formulaire qui sera annexé à la future directive a été soulevée.
Il s’agit plus précisément de la liste des données, notamment biologiques, exigées pour permettre au centre de transplantation d’établir de manière adéquate les risques et avantages de l’opération envisagée.
S’agit-il d’un modèle type, à savoir d’une liste de référence indicative, ou bien d’une liste minimale obligatoire ? Dans cette seconde hypothèse, quelle est alors la latitude des Etats membres pour en adapter l’application ?
Dans la version française de la proposition telle qu’elle a été transmise à la Commission, les deux lectures, sur cette question délicate qui touche aux normes biologiques, étaient a priori possibles.
Le formulaire n’est, en effet, pas prévu par la Commission européenne pour être immuable, puisqu’une disposition prévoit son adaptation et sa mise à jour par comitologie, avec l’intervention du comité de transplantation d’organes, ce qui peut laisser supposer une obligation.
Néanmoins, comme le traité prévoit, comme on l’a vu, la possibilité pour les Etats membres d’introduire ou de maintenir des normes plus strictes en matière de qualité et de sécurité des organes, on devrait en conclure que la seconde lecture était la bonne et que la future directive fixerait un cadre de référence servant ainsi a minima. Cependant, il n’y avait pas de certitude.
Cette question a donc fait, comme l’a souhaité la Commission, l’objet d’une grande attention lors de l’examen au fond du dispositif par le Conseil et le Parlement européen.
En effet, l’adoption du cadre communautaire ne doit pas entraîner, même de manière imprévue, quelque régression que ce soit du niveau des transplantations dans un Etat membre donné. Il ne saurait être question que les niveaux d’excellence atteints par certains pays dans certains domaines puissent être remis en cause.
La solution en définitive dégagée apparaît satisfaisante, avec un dispositif à la fois coordonné et souple reposant sur la distinction entre deux catégories de données : d’une part, les données obligatoires ; d’autre part, les données complémentaires, avec ainsi un pouvoir d’appréciation de l’équipe médicale concernée compte tenu de la disponibilité de l’information et des circonstances particulières du cas d’espèce.
Dans ces conditions, il n’y a pas d’obstacle à l’approbation de la proposition de directive, adoptée en première lecture par le Parlement européen le 19 mai. Elle est inscrite à l’ordre du jour du prochain Conseil « EPSCO » des 7 et 8 juin prochains.
La Commission s’est réunie le 25 mai 2010, sous la présidence de M. Pierre Lequiller, Président, pour examiner le présent rapport d’information.
L’exposé des rapporteurs a été suivi d’un débat.
« Mme François Grossetête. Après cette présentation, je n’ai que peu de choses à dire. C’est un sujet qui est très important pour montrer ce que l'Europe fait concrètement, au service de nos concitoyens. Nos concitoyens comme nous-mêmes ne savons pas ce dont nous pourrons avoir besoin au cours de notre vie. La coordination entre Etats membres est très importante, de même que les normes de sécurité et de qualité et la traçabilité car beaucoup trop de patients décèdent encore faute de greffe.
Pour ce qui concerne le plan d’action, le Parlement européen vient d’adopter un rapport d’initiative qui demande notamment la désignation, dans chaque établissement concerné par les greffes, d’un coordinateur et qui souligne l’importance de l’échange d’informations et des bonnes pratiques. Ce rapport fait également une proposition citoyenne en suggérant un registre de donneurs qui puisse être très rapidement utilisé. Matériellement, le consentement pourrait être mentionné sur le passeport ou le permis de conduire. Pourquoi pas aboutir à un registre en ligne pour aller plus vite ? C’est un élément que l’on peut prendre en compte pour mener une réflexion de fond.
M. Jérôme Lambert, co-rapporteur. C’est effectivement une excellente idée. Certains, en France, font déjà mentionner leur consentement sur leur permis de conduire dans le cadre du volet relatif aux mentions complémentaires. La difficulté est qu’il y a deux systèmes de consentement en Europe, celui du consentement explicite et celui du consentement présumé, et il ne faudrait pas qu’un dispositif européen porte atteinte à notre propre règle dès lors que par manque d’informations ou autres, des donneurs potentiels n’y seraient pas mentionnés. C’est une question sensible car il y a parfois des refus. Mais il ne faut pas implicitement modifier notre règle.
M. Robert Lecou. Le rapport conclut en faveur de la proposition de directive car elle apportera des progrès, c’est essentiel. A-t-on une image précise des différences entre les pays d’Europe et les raisons de ces différences ? Y a-t-il des pays où aucune transplantation n’intervient ?
M. Jérôme Lambert, co-rapporteur. Les études disponibles constatent mais n’expliquent pas les différences. Pour ce qui concerne les prélèvements post-mortem, l’Espagne a des résultats remarquables et la France n’est pas mal placée. Dans certains pays européens, le nombre de transplantations est, c’est vrai, extrêmement réduit. »
La Commission a ensuite approuvé la proposition d’acte communautaire, en l’état des informations dont elle dispose.
ANNEXE :
LISTE DES PERSONNES ENTENDUES PAR LES RAPPORTEURS
ET REMERCIEMENTS
Les rapporteurs tiennent à témoigner leur gratitude aux personnes qu’ils ont rencontrées.
*
* *
Ø Ministère de la santé, des sports et de la vie associative :
– Mme Hélène Esperou, conseillère technique au cabinet de la ministre, pôle politiques de santé et de prévention ;
– M. Vincent Richez, conseiller diplomatique au cabinet de la ministre ;
– M. Maxime Durier, attaché parlementaire au cabinet de la ministre ;
– Mme Roselyne Tardivel, direction générale de la santé ;
– M. Alexandre de la volpiliere, chargé de mission, direction générale de la santé, mission des affaires européennes et internationales.
Ø Agence de la biomédecine :
– Mme Anne Debeaumont, directrice juridique ;
– Dr Karim Laouabdia-Sellami, MD, MPH, directeur médical et scientifique ;
– Dr Pierre Lotty, alors directeur médical et scientifique ;
– Dr Marie Thuong, direction médicale et scientifique.
1 () La composition de cette Commission figure au verso de la présente page.
