
OFFICE PARLEMENTAIRE D'ÉVALUATION DES POLITIQUES DE SANTÉ RAPPORT sur Les résultats du dépistage du cancer du sein par M. Marc BERNIER, Député
INTRODUCTION 7 1. L'OPEPS a vocation à fournir aux parlementaires une expertise en matière de politique de santé 7 2. La saisine de l'OPEPS par la commission des affaires culturelles, familiales et sociales de l'Assemblée nationale et la méthode de travail retenue 8 3. Le dépistage du cancer du sein chez la femme : une action à poursuivre mais qui exige une organisation modernisée 11 TRAVAUX DE L'OFFICE 15 ÉTUDE 17 I.- JUSTIFICATION MÉDICALE ET ÉCONOMIQUE DE LA MISE EN PLACE D'UN PROGRAMME DE DÉPISTAGE DU CANCER DU SEIN 19 A. LES RÉSULTATS DES ESSAIS RANDOMISÉS INTERNATIONAUX 19 1. Les résultats des essais et méta-analyses publiés 19 2. La controverse issue de la méta-analyse de Götzsche et Olsen 20 3. Conclusion 21 B. LES DONNÉES MÉDICO-ÉCONOMIQUES DES ÉTUDES INTERNATIONALES 22 II.- LES MODALITÉS ACTUELLES DU PROGRAMME DE DÉPISTAGE EN FRANCE ET LEURS LIMITES 25 A. ÉTAT DE LA MISE EN PLACE DU PROGRAMME DE DÉPISTAGE ORGANISÉ DU CANCER DU SEIN EN FRANCE AU DÉBUT DE L'ANNÉE 2004 25 1. L'organisation du dépistage au début de l'année 2004 25 2. Le cahier des charges 2001 du programme de dépistage 28 3. Les disparités entre les départements au niveau de la mise en place du dépistage 29 B. LES FINANCEMENTS DU PROGRAMME DE DÉPISTAGE 32 1. Les différents financeurs du programme de dépistage 32 2. La prise en charge des frais correspondant aux actes de mammographie par l'assurance maladie 32 3. La question du remboursement des mammographies effectuées hors du cadre du programme de dépistage 33 C. L'ASSURANCE DE QUALITÉ DU PROGRAMME DE DÉPISTAGE EN FRANCE 34 1. Le contrôle de qualité des appareils mammographiques 34 2. La formation des radiologues et des manipulateurs 35 3. La double lecture 35 4. La double incidence 36 5. L'assurance de qualité au niveau des autres acteurs de la démarche de dépistage : anatomopathologistes et chirurgiens 37 D. LES MOYENS D'ÉVALUATION DU PROGRAMME DE DÉPISTAGE EN FRANCE 37 1. Les organismes impliqués dans l'évaluation 38 2. Les indicateurs disponibles 38 3. Les indicateurs manquants 39 4. Pour une évaluation nationale ou ciblée sur quelques départements ? 40 5. L'observatoire de sénologie 40 5. Le recueil des données économiques 41 6. Le problème posé par le dépistage individuel 41 E. LES MODALITÉS PARTICULIÈRES DU DÉPISTAGE CHEZ LES FEMMES À RISQUE GÉNÉTIQUE 41 1. Généralités 41 2. L'efficacité du dépistage par mammographie dans cette population 42 3. Les modalités actuelles de dépistage chez les femmes à risque génétique 43 4. Les perspectives 43 III.- LES RÉSULTATS DU DÉPISTAGE EN FRANCE ET LEURS INSUFFISANCES 45 A. LES INDICATEURS PRÉCOCES DU DÉPISTAGE POUR L'ANNÉE 2000 45 B. LES RÉSULTATS SUR LA MORTALITÉ PAR CANCER DU SEIN 51 C. LES FACTEURS INFLUENÇANT LA PARTICIPATION DES FEMMES AU PROGRAMME DE DÉPISTAGE ET L'INFORMATION DÉLIVRÉE AUX FEMMES 52 1. Les motifs de non-participation des femmes 52 2. Exemples d'actions ciblées vers les populations exclues du dépistage 54 3. L'importance de la qualité de l'information 54 D. LE RAPPORT COÛT-EFFICACITÉ DU DÉPISTAGE ORGANISÉ EN FRANCE 55 IV.- RÉFLEXIONS SUR L'ÉVOLUTION DE L'ORGANISATION DU DÉPISTAGE EN FRANCE 57 A. LE PROGRAMME DE DÉPISTAGE DU CANCER DU SEIN DOIT-IL ÊTRE ÉTENDU À D'AUTRES CLASSES D'ÂGES ? 57 B. ÉVOLUTION PRÉVISIBLE DE L'ACCESSIBILITÉ AU DÉPISTAGE DU CANCER DU SEIN À MOYEN TERME 59 C. LA PLACE DES ÉTABLISSEMENTS HOSPITALIERS DANS LE PROGRAMME DE DÉPISTAGE ORGANISÉ 60 D. L'AVENIR DU DÉPISTAGE INDIVIDUEL 61 E. VERS DE NOUVELLES TECHNIQUES DE DÉPISTAGE 62 RECOMMANDATIONS 65 ANNEXES 69 ANNEXE 1 : BIBLIOGRAPHIE 71 ANNEXE 2 : COMPOSITION DE L'OFFICE 77 ANNEXE 3 : COMPOSITION DU CONSEIL DES EXPERTS 79 ANNEXE 4 : COMPTE RENDU DE LA RÉUNION DE L'OFFICE DU 2 JUIN 2004 81 Ce rapport relatif aux résultats du dépistage des cancers du sein constitue une véritable novation. Avec le rapport présenté par M. Francis Giraud, sénateur, sur la prévention des handicaps de l'enfant, il s'agit en effet du premier rapport de l'Office parlementaire d'évaluation des politiques de santé (OPEPS). L'OPEPS est une jeune délégation parlementaire. Il est donc utile de rappeler les conditions de sa création avant d'aborder le contenu de la saisine relative au dépistage du cancer du sein. 1. L'OPEPS a vocation à fournir aux parlementaires une expertise en matière de politique de santé La création de l'OPEPS résulte du constat d'une carence de l'expertise parlementaire en matière de politique de santé et d'assurance maladie, plus précisément en ce qui concerne l'évaluation médico-économique de ces politiques. Il vise à compléter la réforme résultant de la loi constitutionnelle du 22 février 1996 et de la loi organique du 22 juillet 1996, qui ont permis au Parlement d'adopter des lois de financement de la sécurité sociale qui « déterminent les conditions générales de son équilibre financier et, compte tenu de leurs prévisions de recettes, fixent ses objectifs de dépenses ». Les décisions publiques en matière de santé reposent sur des données médicales, dont l'analyse et l'exploitation par le Parlement sont difficiles. Le Gouvernement dispose de services qui lui sont directement attachés et peut également recourir à un réseau dense d'agences et d'institutions qui l'alimentent en rapports d'information, d'activité et de réflexion et qu'il peut saisir de tous sujets à dominante « santé » et « santé publique ». Il est apparu que le Parlement souffrait en revanche d'un déficit d'expertise propre. Or, l'expertise nourrit et soutient l'information, condition essentielle à l'exercice des prérogatives de contrôle du Gouvernement et d'élaboration des lois. Cette carence d'expertise en matière d'évaluation en santé se reflète dans le suivi de l'application des lois de financement de sécurité sociale, suivi qui exige des compétences particulières en matière d'évaluation des politiques de santé : les choix sanitaires ont des impacts financiers à court et long terme. Aussi l'office a-t-il pour mission d'informer le Parlement des conséquences des choix de santé publique, afin d'éclairer ses décisions. A cet effet, il recueille des informations, met en œuvre des programmes d'études et procède à des évaluations afin de contribuer au suivi des lois de financement de la sécurité sociale. Cette nouvelle délégation parlementaire a été créée - à la suite d'un amendement de M. Jean-Michel Dubernard, président de la commission des affaires culturelles, familiales et sociales - par l'article 2 de la loi n° 2002-1487 du 20 décembre 2002 de financement de la sécurité sociale pour 2003. La délégation est composée des présidents des commissions de l'Assemblée nationale et du Sénat chargées des affaires sociales ainsi que des rapporteurs de ces commissions en charge de l'assurance maladie dans le cadre des lois de financement de la sécurité sociale et de dix députés et dix sénateurs désignés de façon à assurer, au sein de chaque assemblée, une représentation proportionnelle des groupes politiques. La présidence est assurée alternativement, et pour un an, par le président de la commission chargée des affaires sociales de l'Assemblée nationale (ce fut le cas en 2003) et par le président de la commission chargée des affaires sociales du Sénat (en 2004). L'office est saisi par le Bureau de l'une ou l'autre assemblée (soit à son initiative, soit à la demande d'un président de groupe, soit à la demande de soixante députés ou de quarante sénateurs) ou par une commission spéciale ou permanente. L'office est assisté d'un conseil d'experts composé de six personnalités choisies en raison de leurs compétences dans le domaine de la santé. Le conseil d'experts apporte son concours aux rapporteurs parlementaires pour l'établissement du projet de cahier des charges et la sélection des personnes et organismes proposés pour réaliser les études décidées par l'OPEPS et formule un avis sur la valeur scientifique des travaux réalisés par ces personnes et organismes. En effet, l'office privilégie le recours à des concours extérieurs, sous le contrôle d'un rapporteur parlementaire. 2. La saisine de l'OPEPS par la commission des affaires culturelles, familiales et sociales de l'Assemblée nationale et la méthode de travail retenue La commission des affaires culturelles, familiales et sociales de l'Assemblée nationale a décidé de saisir l'OPEPS sur les résultats du dépistage du cancer. Lors de sa réunion du jeudi 10 avril 2003, l'OPEPS a pris acte de cette saisine et désigné M. Marc Bernier rapporteur. S'intéresser au thème du dépistage du cancer paraissait en effet très opportun dans un contexte marqué par l'adoption du Plan cancer alors que le cancer représente la première cause de décès en France : près de 300 000 personnes apprennent chaque année qu'elles ont un cancer et 150 000 en meurent. Chez les hommes, les trois cancers les plus fréquents sont ceux de la prostate, du poumon et du colon ; chez la femme, ce sont les cancers du sein, du colon et de l'utérus. Quatre de ces cancers - prostate, colon, sein, utérus - sont accessibles à un diagnostic précoce ou à un dépistage. Toutefois, malgré des progrès importants, certains dépistages sont encore insuffisamment développés et il y a des inégalités importantes d'accès. La lutte contre cette maladie a été érigée en priorité par le Président de la République. En outre, le projet de loi relatif à la politique de santé publique a été inscrit à l'ordre du jour du Parlement dès 2003. Comme l'indique la saisine, le but « sera de déterminer quels sont les moyens efficaces de dépistage ou de diagnostic précoce des cancers les plus fréquents, quels sont les programmes efficaces et comment ils peuvent être mis en œuvre. Le rapport servira de base pour faire des propositions d'amélioration ». Le texte de la saisine soulignait bien le souhait des commissaires de disposer de recommandations précises permettant de guider l'action des pouvoirs publics. Conformément à la vocation de l'OPEPS, ces recommandations pourraient, le cas échéant, être prises en compte dès l'automne lors de l'examen du projet de loi de financement de la sécurité sociale pour 2005. L'OPEPS a ensuite défini le cahier des charges de la saisine, en la ciblant sur une sorte de cancer : le cancer du sein. Ce type de cancer paraissait particulièrement adapté à l'objet de la saisine en raison de son incidence croissante et de la montée en charge du dispositif de dépistage dans les départements. En outre, parmi toutes les campagnes de dépistage, le programme de dépistage organisé du cancer du sein est celui qui paraît le plus en avance. Le dispositif pourra être généralisé à tous les départements avant la fin de l'année 2004. La prévention du cancer du sein est d'ailleurs l'un des objectifs de politique de santé publique figurant en annexe du projet de loi relatif à la politique de santé publique : l'objectif à atteindre dans les cinq ans à venir est de réduire le pourcentage de cancers à un stade avancé parmi les femmes, notamment par l'atteinte d'un taux de couverture du dépistage de 80 % pour les femmes de 50 à 74 ans. Le thème de l'organisation et des résultats du dépistage du cancer du sein ayant été sélectionné, l'OPEPS, sur l'avis des membres du conseil des experts, a demandé à la Fédération nationale des centres de lutte contre le cancer (FNCLCC) de réaliser l'étude correspondante. Une réunion de l'OPEPS a été tenue le mardi 14 octobre 2003. Elle a permis aux auteurs de l'étude, les professeurs Alain Brémond et Francis Fagnani, de présenter leurs premières conclusions et la méthode de travail suivie. Faire réaliser par la Fédération nationale des centres de lutte contre le cancer (FNCLCC) une étude particulière sur ce sujet, étude impliquant notamment des essais cliniques, aurait été une opération à la fois bien trop longue et trop coûteuse. Le choix d'une « méta-analyse » 1 et d'une étude fondée sur l'exploitation des références bibliographiques déjà existantes, nationales et internationales, a été fait. L'OPEPS a demandé à la Fédération nationale des centres de lutte contre le cancer (FNCLCC) de structurer l'étude en fonction des deux questions suivantes : Le dépistage du cancer du sein est-il justifié médicalement et économiquement ? Si oui, les modalités de mise en place en France et les résultats sont-ils satisfaisants et à quoi sont dues les insuffisances actuelles ? La FNCLCC devait, enfin, présenter des propositions de recommandations pour l'action publique. Tableau 1
* différence statistiquement significative avec α : 5 %
3. Le dépistage du cancer du sein chez la femme : une action à poursuivre mais qui exige une organisation modernisée La justification du dépistage S'agissant de la première question posée par l'OPEPS, l'étude de la FNCLCC met en évidence la justification médicale des campagnes programmées et régulières de dépistage du cancer du sein. Elles seraient la cause d'une réduction significative de la mortalité par cancer du sein sur les populations étudiées (femmes de plus de cinquante ans et de moins de soixante-neuf ans). Le rapport évalue les coûts par année de vie sauvée entre 5 à 20 000 euros. Il permet de souligner la pauvreté des études existantes sur l'aspect médico-économique des campagnes de dépistage du cancer, en particulier en ce qui concerne les coûts comparés des traitements préventifs et curatifs. En outre, il aurait été intéressant de disposer d'une étude comparée internationale, mettant en évidence les différences de coûts/efficacité entre les principaux pays européens (Allemagne, Royaume-Uni ...). Une évaluation globale du coût du programme de dépistage aurait été également bienvenue. Ce manque participe d'une carence globale d'évaluation relevée par les auteurs du rapport. Trois nuances sont apportées au constat global d'efficacité sanitaire et économique. D'abord, il est précisé que l'analyse des données ne pourra être exhaustive et fiable qu'au moment où le programme de dépistage sera complètement généralisé. Le rapport relève également que les bons résultats obtenus par les recherches exigent des conditions optimales d'organisation, qui ne sont pas nécessairement remplies sur le terrain. Ils soulignent également qu'aucun essai ne permet d'évaluer l'efficacité de la mammographie de dépistage chez les femmes présentant un risque génétique de cancer du sein. L'organisation L'étude effectuée par la FNCLCC aborde ensuite la problématique de l'organisation et du financement des campagnes de dépistage. Le premier constat est celui d'une complexité excessive née de l'enchevêtrement des compétences entre l'Etat, les départements et les régimes de l'assurance maladie. Une autre particularité française est l'absence d'installations radiologiques spécifiques dédiées : tous les mammographes respectant le cahier des charges peuvent participer au programme. Le dépistage organisé repose sur quatre piliers : - il concerne les femmes âgées de 50 à 74 ans ; - il est effectué tous les deux ans, - les dépenses afférentes sont prises en charge à 100 % ; - il est soumis à un contrôle qualité rigoureux : cahier des charges, contrôle des appareils par l'Agence française de sécurité sanitaire des produits de santé (AFSSAPS), formation des opérateurs et double lecture. Les auteurs de l'étude constatent une évaluation insuffisante du dispositif. En particulier, les rares indicateurs existants (taille des tumeurs notamment) ne sont pas standardisés entre les départements. La qualité des données recueillies par les registres est insuffisante. Les résultats L'étude, qui se base sur des données recueillies en 2000, met en évidence l'insuffisante participation des femmes invitées à subir un examen de dépistage, dans le cadre du dépistage organisé. Ce taux se monte à 38 % alors que la préconisation européenne est de 70 %. L'autre point noir est le délai moyen trop long de prise en charge (temps écoulé entre la date du dépistage et celui du premier traitement) : il est de 2,6 mois, alors que la recommandation européenne est de 4 semaines. Le rapport met enfin en évidence le manque de données relatives à l'évaluation économique du ratio coût-efficacité du dispositif. En revanche, le programme français de dépistage organisé du cancer du sein est assez performant s'agissant du taux de rappel, du taux de cancers détectés et de la valeur prédictive de la biopsie. Les préconisations Les auteurs de l'étude ont élaboré une longue liste de recommandations. Trois orientations se dégagent. La première concerne la nécessaire substitution des actions de dépistage organisé au dépistage individuel. L'article L. 321-1 (6°) du code de la sécurité sociale, issu de l'article 81 de la loi n° 2002-303 du 4 mars 2002 relative aux droits des malades et à la modernisation du système de santé, précise que les actions de dépistage sont prises en charge par l'assurance maladie. Le rapport préconise de mieux identifier les actions relevant du dépistage organisé et celles relevant d'actions individuelles, afin de ne prendre en charge que les dépenses engagées lors du dépistage organisé, à l'exception des actions réalisées par les femmes présentant un risque particulier. Favoriser les programmes organisés permettra d'accroître la qualité globale du dépistage et d'en évaluer plus facilement les résultats. L'étude propose également de limiter la prise en charge des dépenses engagées à l'occasion de cet examen de dépistage aux femmes âgées de 50-74 ans et aux femmes présentant un risque particulier, sur la demande argumentée du médecin. L'opportunité de supprimer ou de réduire la prise en charge des examens de dépistage suivant les préconisations mentionnées ci-dessus pourra être discutée dans le cadre de l'examen du projet de loi de financement de la sécurité sociale pour 2005. Les auteurs de l'étude font ensuite un certain nombre de propositions visant à améliorer les conditions d'évaluation du programme organisé. Ils préconisent ainsi de standardiser les indicateurs d'efficacité (par exemple la taille des tumeurs) au niveau régional et national et de faire réaliser une évaluation dans quelques départements ciblés, ce qui permettra d'apprécier la qualité du dépistage et les coûts qui lui sont associés. Il est recommandé que les moyens consacrés à l'établissement des registres des cancers soient augmentés de manière à améliorer les conditions de recueil de ces informations. D'autres propositions concernent l'amélioration de la qualité du programme de dépistage, en particulier en ce qui concerne les appareils utilisés pour réaliser les examens. Elles relèvent notamment de la coopération entre l'ANAES et les sociétés savantes (radiologues, anatomapathologistes) afin de diffuser les bonnes pratiques et de favoriser les regroupements à l'échelon régional plutôt que départemental. D'un point de vue quantitatif, les auteurs de l'étude suggèrent de combler les lacunes en termes d'équipement et d'anticiper les effets de la diminution prévisible des effectifs de radiologues. Enfin, l'organisation du programme doit être modernisée, en informant mieux les femmes concernées et en impliquant plus les médecins généralistes. L'assurance maladie doit améliorer son système d'information afin de pouvoir identifier les dépistages spontanés. * Le rapporteur félicite les auteurs de l'étude pour la qualité de leurs travaux. Il espère que ses collègues trouveront dans ce document une contribution utile, qui pourra alimenter leurs réflexions et leurs interventions lors des débats à venir sur le projet de loi relatif à la politique de santé publique et sur le projet de loi de financement de la sécurité sociale. L'office s'est réuni, le mercredi 16 juin 2004, au Sénat, sous la présidence de M. Nicolas About, sénateur, président, pour examiner le rapport de M. Marc Bernier, député, sur le dépistage du cancer du sein. Un débat a suivi l'exposé de M. Marc Bernier, rapporteur. M. Jean-Michel Dubernard, député, premier vice-président, a estimé qu'il est difficile d'utiliser le véhicule du projet de loi relatif à la politique de santé publique et qu'il faut plutôt envisager l'examen du prochain projet de loi de financement de la sécurité sociale pour tenir compte des propositions faites par le rapporteur. M. Gilbert Barbier, sénateur, a voulu connaître la proportion de femmes qui ont recouru à un examen de dépistage du cancer du sein. Il a observé que des problèmes de coordination pouvaient survenir entre gynécologues et radiologues sur l'opportunité de prescrire un test de dépistage. Dans ces conditions, toute prescription motivée délivrée par un médecin pour subir un test doit être prise en charge par la sécurité sociale. Le rapporteur a indiqué qu'il est très difficile de connaître le nombre de dépistages individuels. Se pose d'ailleurs le problème des effets de seuil autour de la tranche d'âge cinquante - soixante-neuf ans. En tous les cas, le dépistage permet parfois un diagnostic précoce, très important pour parvenir à soigner le cancer du sein. Il a souligné que, en matière de dépistage, tous les experts insistent sur la place et le rôle du médecin généraliste. La proposition qu'il a exposée ne vise qu'à dérembourser les dépistages dits de confort et en aucun cas les actes médicalement justifiés. M Jean-Michel Dubernard, député, premier vice-président, a estimé que les généralistes ne pourraient pas endosser leur rôle sans être soutenus par des spécialistes. Il a indiqué que ce constat plaide en faveur du développement de réseaux regroupant plusieurs professions de santé, cette organisation permettant de favoriser la communication entre les professionnels, de faciliter l'éducation des acteurs et d'assurer une plus grande proximité avec le patient. Le rapporteur a confirmé l'importance qui devait être accordée à la qualité des soins, notamment dans le dépistage du cancer du sein. Il a souligné l'intérêt médical du dépistage organisé par les conseils généraux, l'effet bénéfique de la procédure de double lecture et, quand cela était possible, au recours à la mammographie numérique. Rappelant que son analyse s'inscrit dans une perspective de financement de l'assurance maladie, il a déclaré ne pas avoir d'objection à ce qu'une femme consulte son gynécologue pour faire un diagnostic individuel. Une attention particulière doit être accordée à la collation d'informations statistiques dont l'exploitation est utile pour l'organisation de la politique de dépistage. M. Gérard Dériot, sénateur, a approuvé la nécessité de disposer de statistiques fiables. Il a fait part de l'expérience acquise par le conseil général qu'il préside en soulignant la nécessité de campagnes de sensibilisation régulières en l'absence desquelles la fréquentation des centres de dépistage décroît. M. Jean Bardet, député, a jugé gênant de faire référence à la notion de coût-efficacité comme élément déterminant des politiques de dépistage. M. Nicolas About, sénateur, président de l'OPEPS, a souhaité que des études complémentaires puissent être menées afin d'éclaircir les raisons pour lesquelles le dépistage du cancer du sein devient moins important à partir de soixante-neuf ans. Mme Françoise Forette, membre du comité d'experts, a rappelé les inquiétudes que lui inspire la détermination d'une tranche d'âge spécifiquement visée par le dépistage. Il ne faudrait pas qu'elle conduise à se désintéresser des femmes situées à la marge, notamment celles âgées de plus de soixante-dix ans. M. André Vantomme, sénateur, a également fait part de ses réserves sur la délimitation d'une fourchette d'âge de cinquante à soixante-neuf ans pour le dépistage, susceptible de poser un réel problème d'exclusion de certaines femmes. Il a estimé que la prévention doit s'adresser à tout le monde. * A l'issue de ce débat, l'office a autorisé la publication du rapport.
I.- JUSTIFICATION MÉDICALE ET ÉCONOMIQUE DE LA MISE EN PLACE D'UN PROGRAMME DE DÉPISTAGE DU CANCER DU SEIN 1. Les résultats des essais et méta-analyses publiés Dix études ont été réalisées entre le début des années 1960 et 1990 selon la méthode des essais contrôlés et randomisés pour étudier l'effet du dépistage du cancer du sein sur la mortalité par cancer du sein. Elles ont eu lieu aux Etats-Unis, au Canada, en Suède et au Royaume-Uni. Aucune étude de ce type n'a été menée en France. Si l'on considère les résultats de ces essais pris individuellement (tableau 1), seuls les essais Kopparberg et Edinburg mettent en évidence une réduction statistiquement significative de la mortalité par cancer du sein dans le groupe invité au dépistage par rapport au groupe contrôle. Afin de tenir compte de l'ensemble des données disponibles, plusieurs équipes ont réalisé des méta-analyses dont le résultat est une moyenne pondérée des résultats des différents essais. Parmi celles qui ont été les plus récemment publiées, celle de Humphrey et al. [Humphrey 2002], qui ne prend pas en compte les essais Edinburgh et Malmö II pour des raisons de méthodologie, montre une réduction significative de la mortalité par cancer du sein de 16 % après 14 ans de suivi. La méta-analyse de Nyström et al. [Nystrom 2002] qui ne prend en compte que les essais suédois, c'est-à-dire ceux dans lesquels la mammographie seule est proposée au groupe traité (voir tableau 1), montre une réduction significative de la mortalité par cancer du sein de 21 % après environ 16 ans de suivi. Ces deux résultats concernent des femmes âgées de 40 à 74 ans. La plupart des auteurs ont étudié également l'effet du dépistage mammographique chez les femmes de 40 à 49 ans d'une part et chez les femmes de plus de 50 ans d'autre part. Ces résultats sont à prendre avec précaution puisqu'ils sont issus d'analyses par classe d'âges faites a posteriori et que les essais n'étaient pas construits pour répondre à cette question (sauf pour les essais canadiens). Néanmoins, ils suggèrent fortement que la réduction de la mortalité n'est significative que dans le groupe des femmes de plus de 50 ans. Pour ce groupe, la réduction est de 22 % dans la méta-analyse de Humphrey et al. [Humphrey 2002] et de 35 %, selon les dernières estimations, pour les femmes de 50 à 69 ans dans les essais suédois [International Agency for Research on Cancer 2002]. Au contraire, pour les femmes de 40 à 49 ans, une réduction de mortalité par cancer du sein suite au dépistage n'est pas établie. 2. La controverse issue de la méta-analyse de Götzsche et Olsen La méta-analyse de Götzsche et Olsen publiée en 2000 et 2001 [Gotzsche and Olsen 2000 ; Olsen and Gotzsche 2001a ; Olsen and Gotzsche 2001b] remettait en cause sévèrement les résultats précédents et fut à l'origine d'une vive polémique (Tableau 2). Leurs conclusions reposent sur le classement des différents essais en fonction de leur qualité méthodologique. De ce fait, ces auteurs ont éliminé les essais Malmö II, Edinburgh et Health Insurance Plan dont les données n'étaient selon eux pas exploitables. De plus, pour Götzsche et Olsen, les essais retenus sont trop hétérogènes au niveau méthodologique pour être analysés ensemble (test d'hétérogénéité significatif avec p< 0,05). Pour les auteurs, le résultat global de 20 % de réduction de la mortalité par cancer du sein n'a donc pas de sens et ils ont séparé les essais entre ceux de qualité méthodologique médiocre d'une part et ceux de qualité méthodologique faible d'autre part. Dans le premier groupe, la réduction de mortalité par cancer du sein est non significative. Dans le second, elle est significative et estimée à 32 % (tableau 2). Enfin, pour ces auteurs, le seul critère pertinent pour évaluer le dépistage mammographique est son effet sur la mortalité totale. Ils soulignent que le résultat de la méta-analyse pour ce critère ne montre aucun effet du dépistage par mammographie tout en sachant que les essais n'avaient pas été construits pour étudier l'effet du dépistage sur la mortalité globale. En ce qui concerne le critère de la mortalité totale, l'effet réel est vraisemblablement faible. Nyström et al. montrent une tendance à la réduction de la mortalité totale de l'ordre de 2 % dans les essais suédois [Nystrom 2002]. Par ailleurs, depuis la publication de la méta-analyse de Götzsche et Olsen, un groupe de travail du Centre International de Recherche sur le Cancer [International Agency for Research on Cancer 2002] composé de 24 experts de 11 pays différents a analysé la qualité des essais publiés et les restrictions de Götzsche et Olsen. La conclusion de ce travail est qu'il n'est pas justifié de remettre en cause l'efficacité du dépistage du cancer du sein par mammographie chez les femmes de 50 à 69 ans. Les conclusions d'un congrès ayant eu lieu en juin 2002 à l'Institut Européen d'Oncologie ainsi que celles du rapport de l'ANAES sur ce sujet [Agence nationale d'accréditation et d'évaluation en santé 2002] vont dans le même sens. D'une façon générale, l'existence d'une discordance partielle entre les résultats se focalisant sur la réduction de la mortalité spécifique pour la classe d'âge faisant l'objet du dépistage et l'impact sur la mortalité totale (toutes causes) est un point fréquemment retrouvé dans tout le champ de la prévention et du dépistage. Si cela peut effectivement soulever des interrogations d'ensemble sur l'allocation des ressources au plan macroéconomique du système de santé, cet argument ne peut jusqu'à présent conduire à invalider l'utilité du dépistage du cancer du sein. La question est de savoir si l'absence de mise en évidence d'impact du dépistage organisé du cancer du sein sur la mortalité totale est liée au manque de puissance des études (effectifs trop faibles) ou s'il s'agit d'un impact de santé délétère. Tableau 2 : Résultats de la méta-analyse de Götzsche et Olsen
* différence statistiquement significative avec α : 5 %. Il est donc actuellement admis par la communauté scientifique que le dépistage du cancer du sein par un examen mammographique régulier (tous les 2 ou 3 ans), réalisé dans de bonnes conditions, est justifié médicalement pour les femmes de 50 à 69 ans puisqu'il diminue la mortalité par cancer du sein dans les essais randomisés de 20 à 35 % après plus de 15 ans de suivi. En population générale, les conditions de réalisation d'un dépistage sont néanmoins toujours plus défavorables que celles des essais contrôlés. Les premiers résultats internationaux montrent bien que dans la pratique on est loin d'atteindre la réduction de mortalité spécifique observée dans les essais randomisés. Au Pays-bas, une diminution significative de la mortalité par cancer du sein de 1,67 % par an a été mise en évidence depuis l'introduction du programme de dépistage organisé [Otto 2003]. Ainsi, il est primordial que la rigueur de l'organisation et des normes de qualité avec laquelle les programmes de dépistage sont mis en place dans les différents pays soit maximale pour se rapprocher le plus possible des résultats des essais contrôlés et randomisés. En particulier, le taux de participation des femmes doit être suffisant (en général estimé à plus de 70 %) pour que l'effet soit visible. Enfin, pour mettre en évidence un effet sur la mortalité par cancer du sein, le dépistage doit être évalué rigoureusement et donc organisé. Si l'ensemble de ces éléments n'est pas réuni, la réduction sur la mortalité par cancer du sein peut passer inaperçue. Les études médico-économiques ont pour objectif de mesurer l'efficience du dépistage, c'est-à-dire le ratio entre le bilan des coûts et le bénéfice escompté mesuré généralement en terme de survie gagnée. Les études coût-efficacité du dépistage du cancer du sein réalisées au niveau international aboutissent à des résultats différents selon les pays. En effet, ces résultats sont influencés par beaucoup de facteurs tels que la sensibilité du test, les données épidémiologiques locales, les modalités de l'organisation du dépistage, le coût général des soins, les traitements utilisés ou encore la méthodologie de l'analyse. Par ailleurs, les résultats de ces études sont basés sur un ensemble d'hypothèses, en particulier concernant l'histoire naturelle de la maladie. Ils sont donc à interpréter avec précaution. Les études publiées reposent généralement sur des données économiques recueillies dans le cadre de programmes existants et sur des modèles de simulation pour l'estimation des bénéfices en mortalité. Cette dernière méthode, bien que caractérisée par un niveau de preuve inférieur à celui des approches expérimentales, est actuellement largement reconnue et utilisée. Il s'agit en effet de la seule approche méthodologique possible qui permette de comparer les ratios coût-efficacité de différentes stratégies de dépistage compte tenu de l'impossibilité pratique de réaliser des études expérimentales pour répondre à toutes les questions posées. Quelle que soit la méthode utilisée, et malgré les divergences entre les pays, il apparaît que le dépistage du cancer du sein constitue dans les pays développés d'Europe occidentale un dispositif efficient de santé publique pour la tranche d'âge 50-69 ans. Les coûts par année de vie supplémentaire gagnée grâce au dépistage sont de l'ordre de 5 à 20 000 euros selon les hypothèses retenues pour la tranche d'âge 50-69 ans ce qui correspond à un ordre de grandeur tout à fait raisonnable en comparaison à de très nombreuses actions mises en œuvre couramment pour réduire la mortalité par cancer dans le système de soins. Par contre, le ratio coût par année de vie gagnée augmente considérablement si l'on modélise l'extension du dépistage aux tranches d'âge inférieures ou supérieures. Conclusion générale : Le dépistage du cancer du sein est a priori justifié médicalement et économiquement pour la tranche d'âge des femmes de 50 et 69 ans. En pratique, cette justification exige une grande rigueur dans la réalisation des programmes de dépistage de masse afin de rapprocher leurs conditions d'exercice de celles des programmes expérimentaux qui l'ont fondée. A. ÉTAT DE LA MISE EN PLACE DU PROGRAMME DE DÉPISTAGE ORGANISÉ DU CANCER DU SEIN EN FRANCE AU DÉBUT DE L'ANNÉE 2004 1. L'organisation du dépistage au début de l'année 2004 L'organisation actuelle du programme de dépistage du cancer du sein est répartie en 3 niveaux : national, régional et départemental. Le rôle de l'Etat, réaffirmé dans la dernière loi de santé publique discutée à l'Assemblée nationale en octobre 2003, est de définir la politique de santé publique et en particulier la liste des programmes de dépistage des cancers en accord avec l'ANAES (Agence nationale d'accréditation et d'évaluation en santé) et l'assurance maladie. Il définit au niveau de l'Institut national du cancer, via le comité national du cancer et les groupes techniques spécifiques à chaque type de cancer dépisté, les stratégies de mise en œuvre du plan national de lutte contre le cancer et rédige les cahiers des charges associés au dépistage. Actuellement, le programme de dépistage du cancer du sein est le plus en avance dans la mise en place. Pour ce programme, le dernier cahier des charges date de 2001 (arrêté du 27 septembre 2001). La mise en œuvre du programme de dépistage est au contraire décentralisée et est à la charge des départements. Chaque département participant au programme a une structure de gestion du dépistage qui assure essentiellement : - l'information et la sensibilisation des femmes ciblées par le programme ; - l'information et la sensibilisation des médecins ; - l'invitation des femmes de la population cible ; - les relations entre les professionnels de santé et les personnes dépistées pour le recueil des résultats des tests ; - le recueil des résultats des tests et des données épidémiologiques permettant l'évaluation du programme de dépistage ; - l'assurance qualité du programme (vérification du suivi du cahier des charges par les radiologues, double lecture...). Ces structures mises en place initialement pour le dépistage du cancer du sein pourront également gérer la mise en place d'autres programmes de dépistage (ex : cancer colo-rectal et cancer du col de l'utérus). C'est déjà le cas à titre d'essai dans certains départements (ex : Isère). Au niveau régional, les directions régionales des affaires sanitaires et sociales assurent un contrôle de la cohérence des programmes de dépistage avec les programmes régionaux de santé et les programmes régionaux d'accès à la prévention et aux soins. Elles sont également garant de la qualité des programmes départementaux de dépistage, définissent les besoins de formation des professionnels et participent à la mise en place de ces formations. De même, elles mettent en œuvre l'appel à candidature des structures de gestion, examinent les candidatures et participent à l'évaluation du programme de dépistage. Le schéma 1 récapitule les différents acteurs du programme de dépistage. Il fait ressortir la complexité et la lourdeur du dispositif à laquelle s'ajoute le fait que le programme de dépistage implique la participation de plusieurs centaines de cabinets de mammographie ainsi qu'un grand nombre de laboratoires d'anatomocytopathologie. En effet, une des particularités françaises est que le programme de dépistage organisé du cancer du sein ne repose pas sur des installations radiologiques spécifiques mais potentiellement sur tous les mammographes respectant le cahier des charges imposé par le programme. Les mammographies de dépistage sont essentiellement réalisées dans les cabinets libéraux de radiologie. A titre d'exemple, en région Rhône-Alpes, l'estimation du pourcentage de mammographies réalisées en cabinet libéral est comprise entre 70 et 79 % (étude ORS Rhône-Alpes mars 2002). Enfin, il demeure une ambiguïté entre les rôles respectifs de l'Etat central et des services déconcentrés de l'Etat en région qui doit être clarifiée. Schéma 1 : Organisation du dépistage du cancer du sein en France 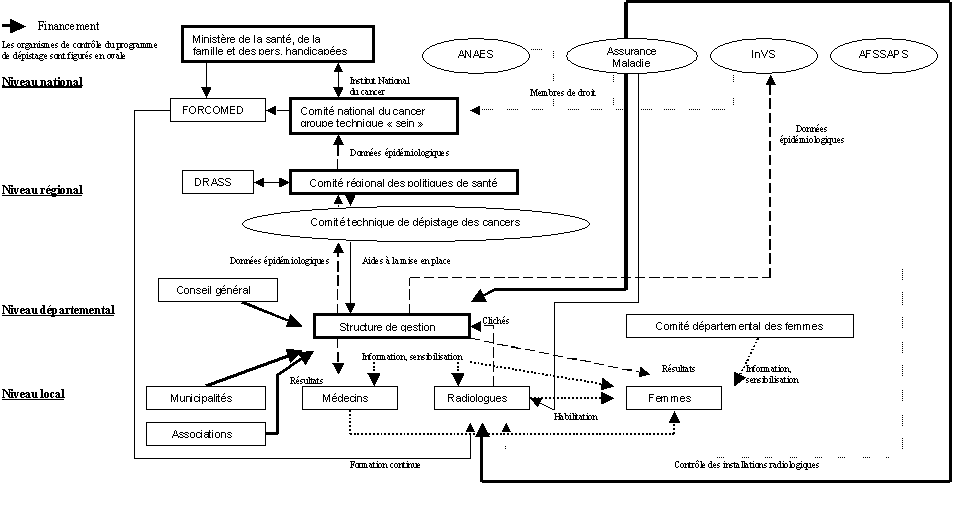 2. Le cahier des charges 2001 du programme de dépistage Le programme actuel de dépistage organisé du cancer du sein s'adresse aux femmes de 50 à 74 ans. Celles-ci reçoivent tous les deux ans une invitation pour une mammographie chez un radiologue conventionné avec l'assurance maladie pour le dépistage ainsi qu'un bon de prise en charge à 100 % de l'examen. La mammographie doit être effectuée selon deux incidences par sein (face et oblique externe). En cas d'absence d'anomalie ou d'anomalie bénigne, les clichés sont adressés à la structure de gestion pour une deuxième lecture dans le but de limiter le nombre de faux négatifs. Les résultats doivent ensuite être envoyés aux femmes et à leur médecin traitant dans un délai de 15 jours maximum. En cas de détection d'une anomalie à la première lecture, le radiologue peut réaliser immédiatement des examens supplémentaires (cliché supplémentaire, échographie) pour affiner le diagnostic. Si le bilan reclasse l'anomalie en bénin, les clichés bénéficieront également d'une deuxième lecture. Les radiologues doivent par ailleurs utiliser la classification Bi-Rads de l'American College of Radiology (ACR) adaptée par l'ANAES pour décrire les images de mammographie dont le but est de standardiser les interprétations radiologiques. Depuis le cahier des charges de 2001, l'examen mammographique doit être systématiquement associé à un examen clinique dont l'objectif est également de réduire le nombre de faux négatifs (cas des cancers palpables et radiologiquement occultes). Une des caractéristiques fondamentales du dépistage organisé est qu'il est soumis à un contrôle de qualité rigoureux tant au niveau du matériel utilisé qu'au niveau des formations du personnel médical (Ce point sera détaillé dans le chapitre 2C). Ce n'est qu'à cette condition que les radiologues libéraux ou les établissements de santé peuvent établir une convention avec les organismes d'assurance maladie. Les radiologues exerçant dans un établissement public de santé ou dans un établissement participant au service public hospitalier sont tenus de respecter les mêmes procédures d'assurance de qualité que les radiologues libéraux pour pouvoir participer au programme de dépistage. Enfin, le programme national de dépistage fait l'objet d'une évaluation de son efficacité à l'échelle nationale. Les données épidémiologiques sont recueillies au niveau des structures de gestion. Elles sont transférées à l'Institut de veille sanitaire (InVS) qui a en charge cette évaluation et publie après contrôle un rapport annuel où figurent les résultats nationaux et départementaux. Dans l'état actuel de la mise en place du programme de dépistage organisé, l'évaluation n'est pas une priorité et reste le parent pauvre du dispositif. Nous y reviendrons au chapitre 2D. Ce dernier cahier des charges, datant de 2001, tente en particulier de répondre à plusieurs insuffisances de l'organisation précédente (persistance importante du dépistage non organisé, désengagement des médecins dans le programme...) et permet d'ajuster le programme de dépistage sur les dernières recommandations scientifiques. Il a néanmoins quelques inconvénients. En effet, contrairement à l'organisation du précédent cahier des charges, les clichés de mammographie ne sont plus archivés par la structure de gestion mais sont donnés aux femmes. Ceci ne permet pas facilement une analyse a posteriori des cancers de l'intervalle. Par ailleurs, en cas de détection d'une anomalie, la deuxième lecture a été supprimée. Cette mesure permet certes d'éviter des reconvocations inutiles et de diminuer l'angoisse liée à un diagnostic incertain (dépêche APM du 08/04/2004 concernant une étude réalisée à Bethesda), mais elle peut potentiellement induire une augmentation du nombre de faux positifs. En outre, les procédures du cahier des charges de 2001 sont plus complexes ce qui augmente la charge de travail des structures de gestion [Séradour 2004]. Enfin, une récente enquête réalisée par l'Institut national de la consommation (60 millions de consommateurs d'avril 2004) montre que le cahier des charges décrit ci-dessous n'est pas appliqué par certains médecins et pointe ainsi les limites d'un dispositif dans lequel il n'existe aucun moyen d'obligation et ni de sanction. 3. Les disparités entre les départements au niveau de la mise en place du dépistage Au niveau de l'ancienneté de la mise en place du programme de dépistage organisé La première disparité entre les départements concerne l'ancienneté de leur implication dans le programme national (carte 1). Les expériences pilotes menées par la CNAMTS ont été mises en place à partir de 1985 dans le Rhône, dans le Bas-Rhin puis à Montpellier. Puis rapidement, d'autres départements ont pris part au programme de dépistage pour atteindre 10 départements impliqués fin 1991. Une deuxième vague d'extension a eu lieu à la création du comité national de pilotage en 1994 alors qu'un premier cahier des charges a été publié en 1996 par la cellule de gestion du Programme national de dépistage systématique du cancer du sein. Néanmoins la progression de l'extension à l'ensemble du territoire a été très lente jusqu'à fin 2000, où seulement 32 départements étaient impliqués dans la démarche. Au contraire, avec le Plan cancer présenté par la DGS en 2003 à l'initiative du Président Jacques Chirac et l'affectation de budgets supplémentaires, l'extension du programme de dépistage a accéléré fortement en 2003. Entre janvier et octobre 2003, 35 départements ont entamé la mise en place du programme de dépistage et, au 30 avril 2004, 98 départements ont effectivement une structure de gestion et envoyé leurs premières invitations. La Guadeloupe devrait entrer dans le dispositif en juin 2004 et la Guyane à la fin de l'année 2004. Les territoires d'outre-mer ne font pas l'objet de la généralisation du programme de dépistage. Au niveau de l'organisation du dépistage La mise en œuvre au niveau départemental du programme de dépistage du cancer du sein fait néanmoins apparaître des disparités parfois importantes entre les départements au niveau de l'organisation comme des résultats. A titre d'exemple, l'InVS a pointé de grandes différences dans le délai entre la date de dépistage et la date d'envoi des résultats d'une part et la date du premier traitement en cas de diagnostic positif d'autre part. Ces écarts peuvent être dus à des différences dans l'organisation du circuit des clichés ou dans la fréquence des séances de deuxième lecture qui dépend directement du nombre de deuxièmes lecteurs et du matériel disponible [Institut national de veille sanitaire 2000]. Il pourrait être intéressant d'envisager une organisation régionale des centres de deuxième lecture pour palier au manque d'experts de certains départements ; Par ailleurs, certains départements ont développé un système de triple lecture en cas de désaccord entre les deux premiers lecteurs. D'autres enfin (Aveyron, Hérault, Orme) utilisent des installations mobiles (mammobiles) pour améliorer l'accessibilité du dépistage. Toutefois, les données les plus récentes dont on dispose sur ces problèmes d'organisation datent de l'année 2000 et ne reflètent donc peut-être plus la situation actuelle. Au niveau de la répartition géographique des mammographes Actuellement, le seul moyen d'avoir une estimation globale de la répartition des sites de dépistage est de recenser auprès des structures de gestion le nombre de radiologues agréés pour le dépistage organisé par départements. Nous avons donc effectué un sondage auprès de toutes les structures de gestion ouvertes en janvier 2004. Sur les 93 structures contactées, le taux de réponse au sondage a été de 91 % et parmi les non-réponses, deux correspondent à un refus de participation au sondage. L'analyse de ces données fait apparaître, qu'à la fin du premier trimestre 2004, la densité moyenne de radiologues habilités pour le programme national de dépistage est de 5,55 radiologues pour 10 000 femmes et que la densité moyenne de cabinets de mammographie habilités pour le programme de dépistage est de 2, cabinets pour 10 000 femmes. Il existe de très grandes variations de ces taux entre les départements (exemple : 2,59 radiologues habilités pour 10 000 femmes dans le Cantal contre 10,00 en Seine-Saint-Denis) mais la seule différence d'ancienneté de mise en place du programme de dépistage ne suffit pas à expliquer ces inégalités. Certains départements très récemment entrés dans la démarche de dépistage, comme la Gironde, la Haute-Garonne, la Haute-Corse ou l'Aude ont déjà atteint une densité de radiologues habilités supérieure à la moyenne nationale alors que pour d'autres départements la mise en place est plus lente (exemple : Hautes-Alpes, Creuse). Etant donné que la mise en place d'un programme de dépistage au niveau départemental repose pour beaucoup sur la motivation des acteurs impliqués localement, il paraît donc important de soutenir le travail initié en particulier dans les départements où la mise en œuvre est la plus laborieuse pour garantir sa pérennisation. Par ailleurs, le sondage réalisé met en évidence que dans 14 des départements ayant répondu au questionnaire, le nombre de cabinets de mammographie est très limité (inférieur ou égal à 5). Ces départements font certes partie de ceux ayant initié le programme de dépistage en 2003 mais cela laisse supposer des difficultés importantes d'accès la mammographie au moins dans un premier temps. Afin de mieux contrôler cette question de l'accès à la mammographie en France, l'AFSSAPS effectuera, au cours de l'année 2004, une inspection de l'ensemble des installations mammographiques pour être en mesure d'établir la cartographie complète des appareils avec leur niveau de qualité. 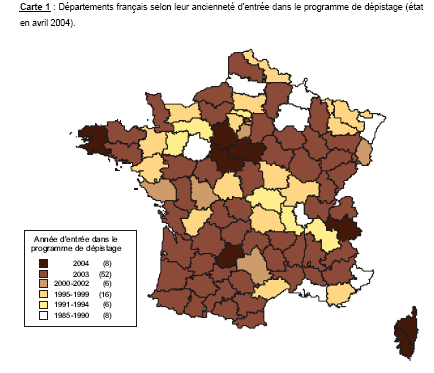 1. Les différents financeurs du programme de dépistage L'organisation décentralisée du programme de dépistage français va de paire avec une répartition de la prise en charge financière du programme. Au niveau national, le comité national du cancer et bientôt l'Institut national du cancer sont financés par l'Etat. En 2003, l'Etat a, de plus, débloqué pour le Plan Cancer 30 millions d'euros complémentaires pour garantir l'extension du programme de dépistage à tout le territoire. Dans ce cadre l'Institut de veille sanitaire (InVS) chargé de l'évaluation du programme de dépistage reçoit de l'Etat des budgets importants, mais ceux-ci ne sont pas conçus pour permettre l'embauche de personnel en contrat à durée indéterminée. Cette impossibilité d'avoir des postes pérennes est un obstacle au bon fonctionnement de l'évaluation du programme de dépistage organisé. Au niveau régional, la Direction régionale des affaires sanitaires et sociales (DRASS) et le comité régional des politiques de santé financent leurs actions au sein du programme de dépistage (homogénéisation des programmes départementaux, campagnes de sensibilisation, formation...). Au niveau départemental, les conseils généraux et les organismes de l'assurance maladie assurent le financement des structures de gestion. Les organismes mutualistes, les autres collectivités locales ou territoriales, les associations d'usagers ou de malades ou les établissements de santé à but non lucratif peuvent également apporter leur soutien financier. Par ailleurs, la loi sur la décentralisation permet désormais à l'Etat de se substituer aux départements réticents à la mise en place du programme de dépistage. En ce qui concerne le matériel, 80 % de mammographes français appartiennent au domaine libéral. L'achat et le contrôle de qualité de la majorité des appareils demeurent donc à la charge des radiologues de ce secteur. 2. La prise en charge des frais correspondant aux actes de mammographie par l'assurance maladie Les actes de mammographie entrant dans le cadre du programme de dépistage sont pris en charge à 100 % par l'assurance maladie et un bon de prise en charge envoyée aux femmes avec leur invitation leur évite d'avancer les frais correspondants. Par ailleurs, l'assurance maladie verse aux radiologues systématiquement 4 euros par mammographie lue en deuxième lecture. - les mammographies réalisées dans les établissements de santé publics ou dans les établissements participant au service public hospitalier En participant au programme de dépistage, les établissements de santé publics et les établissements participant au service public hospitalier s'engagent à ne pas demander d'avance de frais aux femmes se présentant pour une mammographie de dépistage (note DHOS/DGS du 3 novembre 2003). Depuis le 1er janvier 2004, ces établissements reçoivent une dotation nouvelle hospitalière pour l'activité de dépistage (note DHOS/DGS du 3 novembre 2003). - Les mammographies réalisées dans les cabinets libéraux de radiologie Les organismes d'assurance maladie remboursent les radiologues selon un tarif forfaitaire. Ne sont pris en charge à 100 % que les actes correspondant au dépistage. Les examens supplémentaires type échographie suivent les modalités classiques de paiement à savoir avance de frais par la patiente et prise en charge à 70 % par l'assurance maladie. Depuis la signature de l'accord sur le bon usage des soins, les tarifs de toutes les mammographies sont identiques (66,42 euros) et cet acte est côté ZM41 dans la nomenclature des actes professionnels. Cet accord stipule également qu'à partir du janvier 2005, une réduction de 5Z sera appliquée pour toute mammographie réalisée par un radiologue ne participant pas au programme de dépistage organisé. Cette mesure a pour objectif d'inciter les radiologues à participer au programme de dépistage et de supprimer le dépistage individuel d'ici 2006 afin de garantir une qualité maximale de l'activité mammographique sur l'ensemble du territoire. 3. La question du remboursement des mammographies effectuées hors du cadre du programme de dépistage Le système actuel ne permet pas de différencier au niveau de l'assurance maladie les mammographies de dépistage et les mammographies de diagnostic et parmi les mammographies de dépistage celles qui entrent dans le cadre du programme de dépistage organisé et les autres. Or se pose la question du remboursement des mammographies de dépistage effectuées dans le cadre du dépistage individuel, c'est-à-dire sans les garanties de qualité associées au dépistage organisé en particulier sans double-lecture et avec une périodicité non contrôlée. Ces mammographies concernent en particulier des femmes de moins de 50 ans ou des mammographies de dépistage dont la périodicité est inférieure à 2 ans. Afin d'assurer la cohérence entre les objectifs de santé publique poursuivis par l'organisation du dépistage dans la tranche d'âge 50-74 ans et la gestion du risque-maladie, il serait sans doute souhaitable de limiter le remboursement des mammographies de dépistage à la seule tranche d'âge 50-74 ans (lorsqu'elles sont effectuées à un rythme d'une fois tous les deux ans) ainsi qu'aux indications de dépistage lié à des antécédents familiaux ou un risque génétique élevé (sans restriction d'âge). Plus précisément, les mammographies entrant dans le cadre du programme de dépistage organisé seraient remboursées à 100 % par l'assurance maladie. Les mammographies de dépistage chez les femmes présentant un risque génétique ou présentant une pathologie mammaire bénigne le seraient aussi sur demande argumentée du médecin via un système de notification. Pour toutes les autres mammographies de dépistage, le remboursement serait de 0 %. Ce mécanisme de notification, basé sur la responsabilisation des professionnels, n'est pas simple à mettre en place et demande un contrôle a posteriori de la prescription par l'assurance maladie. Il est d'ores et déjà techniquement faisable car prévu dans la loi de la sécurité sociale. Il permettrait, en outre, d'éviter la lourdeur du mécanisme d'entente préalable. Le programme de dépistage organisé du cancer du sein est associé à un dispositif d'assurance de qualité strict en particulier au niveau de la pratique de la mammographie. Ce dispositif est basé sur les « lignes directrices européennes sur l'assurance qualité en matière de dépistage » dont la dernière mise à jour date de juillet 2001. C'est l'Etat qui a la responsabilité de veiller à l'assurance qualité et à la sécurité du programme de dépistage (arrêté du 27 septembre 2001 publié au JO du 3 octobre 2001). 1. Le contrôle de qualité des appareils mammographiques Pour détecter des tumeurs à des stades précoces tout en limitant la dose de radiations ionisantes reçue au cours d'une mammographie, il est indispensable que la qualité technique de l'appareil utilisé soit optimale. C'est à l'Agence française de sécurité sanitaire des produits de santé (AFSSAPS) que revient la charge de définir les modalités du contrôle de qualité des installations de mammographie. Une décision du 27 mars 2003 du directeur général de l'AFSSAPS, entrée en vigueur le 8 octobre 2003, fixe ces modalités pour les appareils analogiques, qui sont pour le moment les seuls appareils habilités pour le programme de dépistage organisé. Il est à noter que ce référentiel s'applique non seulement aux appareils utilisés dans le cadre du programme de dépistage mais à tous les mammographes analogiques exploités en France soit environ 3 000 appareils en 2003. Le contrôle de qualité comporte un volet contrôle de qualité externe, effectué tous les 6 mois par une société agréée par l'AFSSAPS, et un volet contrôle de qualité interne, effectué quotidiennement, ou de façon plus espacée selon les caractéristiques contrôlées, par le personnel local. A l'issue de la visite de la société de contrôle, un rapport est remis à l'AFSSAPS qui doit veiller à ce que le radiologue prenne les mesures correctives éventuellement nécessaires. La structure de gestion reçoit un certificat de visite attestant que le radiologue a fait son contrôle de qualité. De même, le cahier colligeant les résultats des mesures quotidiennes est mis à la disposition de l'AFSSAPS pour contrôle. 2. La formation des radiologues et des manipulateurs Pour participer au programme de dépistage, les radiologues s'engagent à participer à des formations spécifiques validantes qui leur sont proposées. De même, les manipulateurs effectuant des mammographies doivent suivre une formation spécifique. Ces formations sont assurées par l'association FORCOMED. Fin mars 2004, 3 835 radiologues avaient été formés en lecture et assurance qualité sur les 6 850 radiologues exerçant en France (estimation de la Fédération Nationale des Médecins Radiologues). De plus, 3 429 manipulateurs ont été formés en assurance qualité et 3 620 en organisation du dépistage. Par ailleurs, les radiologues doivent s'engager à effectuer un minimum de 500 mammographies par an pour participer au programme de dépistage. Ce chiffre de 500 mammographies par an, relativement empirique, reprend celui des recommandations de l'American College of Radiology et non celui des recommandations européennes qui fixent ce seuil à 5 000 mammographies par an. Tous les clichés négatifs en première lecture, c'est-à-dire ceux qui sont considérés par le premier lecteur comme ne présentant aucune anomalie ou avec une anomalie bénigne, sont envoyés à la structure de gestion pour une deuxième lecture dans un délai de quelques jours. Cette deuxième lecture doit se faire de manière centralisée lors de séances organisées au sein de la structure de gestion. Pour des raisons géographiques, un deuxième centre de deuxième lecture peut être autorisé. De plus, une troisième lecture peut éventuellement être organisée par la structure de gestion si le taux de positifs du deuxième lecteur paraît trop élevé. Les radiologues deuxièmes lecteurs doivent avoir reçu une formation spécifique, réaliser au moins 500 mammographies par an et s'engagent à en lire 2 000 par an. Plusieurs équipes ont étudié l'influence de la double lecture sur la sensibilité de la mammographie et sur le taux de rappel des femmes. Selon les études, l'augmentation de la sensibilité va de 5 à 15 % [Anttinen 1993 ; Séradour 1997 ; Brancato 2000 ; Ciatto 1995 ; Thurfjell 1994] grâce à la double lecture. Cette augmentation s'accompagne souvent de l'augmentation du taux de rappel [Brancato 2000 ; Brown 1996] sauf dans les cas où la double lecture est associée à la recherche d'un consensus entre les 2 lecteurs en cas de résultats discordants [Anttinen 1993 ; Brown 1996]. Le coût de la double lecture a été évalué dans une étude finlandaise à une augmentation de 39 % par cancer détecté [Leivo 1999]. Dans l'étude de Brown et al. (Royaume-Uni), le coût de la double lecture sans recherche de consensus est plus élevé que le coût d'une simple lecture alors que le coût de la double lecture avec recherche de consensus est inférieur à celui d'une simple lecture [Brown 1996]. En France, une évaluation du coût de la double lecture a été réalisée dans les Bouches du Rhône entre 1990 et 1995 [Séradour 1997] et a abouti au fait que le surcoût correspondant (5 % de l'ensemble des coûts) était justifié au vu des bénéfices sur la sensibilité du dépistage. Double lecture d'une part, formation et expérience des radiologues d'autre part sont deux facteurs clés permettant de limiter les nombres de faux positifs et de faux négatifs de la mammographie. A titre d'exemple, le nombre de faux positifs aux Etats-Unis est environ deux fois plus élevé qu'au Royaume-Uni [Smith-Bindman 2003]. Selon ces auteurs, une des explications possibles serait qu'aux Etats-Unis l'habilitation des radiologues pour le dépistage est accordée à partir de 480 mammographies par an et que la double lecture y est peu pratiquée alors qu'au Royaume-Uni les radiologues doivent lire au minimum 5 000 mammographies par an et que la double lecture est pratiquée dans 90 % des cas. En France, les clichés positifs en première lecture ne sont pas soumis à une deuxième lecture sauf si les clichés ou examens complémentaires réalisés dans la foulée se révèlent négatifs. Depuis la mise en place du cahier des charges de 2001 et selon les recommandations de l'ANAES, toutes les mammographies dans le cadre du programme de dépistage se font selon deux incidences par sein (cranio-caudale et oblique externe). Même si les résultats publiés à ce sujet sont parfois divergents, une étude randomisée réalisée en Angleterre a montré que l'utilisation de deux incidences au lieu d'une augmentait la sensibilité de la mammographie de 24 % et réduisait le taux de rappel de 15 % lors de la première vague de dépistage [Wald 1995]. Pour les mammographies suivantes, aucune étude n'a été publiée. Sur la base de ces résultats complétés par ceux d'études rétrospectives, l'ANAES recommande donc de pratiquer deux incidences par sein au moins pour les deux premières vagues de dépistage [Agence nationale d'accréditation et d'évaluation en santé 1999]. 5. L'assurance de qualité au niveau des autres acteurs de la démarche de dépistage : anatomopathologistes et chirurgiens Les effets positifs du dépistage reposent sur la qualité de toutes les étapes de la prise en charge et pas uniquement sur celle de l'acte mammographique. Il est donc indispensable d'assurer également la qualité de la prise en charge des lésions détectées. Dans ce cadre, des bonnes pratiques chirurgicales décrites dans le rapport « Chirurgie des lésions mammaires : prise en charge en première intention » publié en octobre 2002 par l'ANAES sont en cours de diffusion. En ce qui concerne les données anatomocytopathologiques (nomenclature, procédure de mesure de la taille de la tumeur), leur standardisation n'est pas encore effective. Les réseaux d'anatomopathologistes prévus par le cahier des charges du programme national ont cet objectif. Leur mise en place varie beaucoup d'un département à l'autre y compris parmi ceux qui ont pris part au dépistage organisé depuis plusieurs années. Un travail en cours sous l'égide de la mission interministérielle de lutte contre le cancer va également dans ce sens. Néanmoins, la standardisation des données anatomocytopathologiques ne doit pas se limiter au niveau départemental. Il est essentiel qu'elle soit précédée d'une standardisation au niveau national puis régional afin, en particulier, de définir clairement les indicateurs d'efficacité du programme de dépistage. Il serait donc préférable que les réseaux anatomocytopathologiques soient organisés à l'échelle régionale. Ceci est déjà en cours en région Rhône-Alpes. L'objectif du dépistage organisé du cancer du sein est de diagnostiquer des cancers invasifs de dimension infraclinique à un coût acceptable. Il est donc essentiel pour en suivre la mise en place de disposer d'indicateurs permettant d'évaluer l'efficacité du dispositif d'une part et son coût d'autre part. Ces indicateurs doivent être définis très clairement pour permettre l'évaluation de l'efficacité du dépistage dans tous les départements de façon homogène. De même les écarts tolérables au niveau de ces indicateurs entre les départements doivent être fixés a priori. 1. Les organismes impliqués dans l'évaluation L'Institut de veille sanitaire (InVS) a en charge l'évaluation scientifique et épidémiologique du programme de dépistage aussi bien à court terme afin de contrôler et éventuellement d'ajuster sa mise en œuvre qu'à long terme en étudiant son impact sur la mortalité. Les aspects organisationnels et administratifs sont évalués par la Direction générale de la santé avec l'aide du groupe technique national sur le dépistage du cancer du sein. Les structures de gestion départementales ont la charge de recueillir les données épidémiologiques demandées par l'InVS pour l'évaluation annuelle du programme de dépistage organisé. Ces données comportent l'âge des femmes, leurs antécédents de mammographie, le résultat de la mammographie et les résultats anatomo-pathologiques des cancers détectés. Elles sont utilisées dans un premier temps au niveau local dans le but d'établir des statistiques individuelles et globales permettant à chaque médecin d'évaluer sa pratique. Dans un deuxième temps, les données sont envoyées aux organismes d'assurance maladie et à l'InVS. Ce dernier publie annuellement les indicateurs précoces d'efficacité du programme de dépistage aux niveaux national et départemental. 2. Les indicateurs disponibles Les indicateurs qui sont calculés annuellement par l'InVS à partir de ces données sont indiqués dans le tableau 3. Ces indicateurs permettent de suivre la mise en place du programme de dépistage et éventuellement d'en ajuster les modalités. Ils fournissent également des éléments de réponse quant à l'efficacité du programme de dépistage en attendant d'avoir suffisamment de recul pour pouvoir étudier son impact sur la mortalité par cancer du sein (au moins 10-15 ans). Deux des principaux indicateurs d'efficacité du dépistage sont le nombre de tumeurs infracliniques détectées et le nombre de cancers invasifs détectés. Or on ne dispose actuellement d'aucune définition précise au niveau national de ces indicateurs. Il est urgent de standardiser leur définition en précisant notamment la méthode de mesure de la taille des tumeurs et les critères anatomocytopathologiques des cancers invasifs. Ces définitions doivent ensuite être diffusées à l'ensemble des laboratoires d'anatomocytopathologie et leur utilisation doit faire l'objet d'un contrôle. Ce travail de concertation est en discussion depuis de nombreuses années mais n'a toujours pas abouti. Il est urgent que ce manque soit comblé rapidement par la profession pour assurer une évaluation de qualité. Tableau 3 : indicateurs calculés annuellement par l'InVS
D'autres indicateurs sont essentiels à l'évaluation d'un programme de dépistage. Il s'agit en particulier du taux de faux négatifs et du taux de cancers de l'intervalle. Il s'agit des cancers découverts dans l'intervalle entre deux examens de dépistage soit parce qu'ils étaient alors invisibles soit parce qu'ils sont passés inaperçus. Pour obtenir ces données, il est nécessaire d'avoir accès à l'ensemble des cancers du sein qui se sont développés dans la tranche d'âges considérée. Ces données peuvent être obtenues en collaboration avec les registres du cancer et les anatonomo-pathologistes. L'InVS travaille actuellement sur l'organisation de la transmission systématique des données anatomocytopathologiques vers les structures de gestion ainsi que sur celle de la transmission des données des registres vers les structures de gestion. Ces deux sources d'informations sont complémentaires puisque les recueils anatomopathologiques sont disponibles relativement rapidement alors que les registres, plus exhaustifs, sont généralement disponibles avec un délai de 3 ans. Enfin, les radiothérapeutes pourraient représenter une autre source d'information précieuse, et disponible relativement rapidement, puisque presque tous les cancers invasifs bénéficient d'une radiothérapie. L'estimation de l'efficacité du programme de dépistage peut également se faire en étudiant l'évolution de l'incidence des stades des cancers détectés parmi les femmes participant au dépistage. En effet, le nombre de cancers de mauvais pronostic (cancers métastatiques d'emblée) devrait théoriquement avoir tendance à diminuer si le dépistage organisé permet de détecter des tumeurs plus précocement. Or, les données dont nous disposons actuellement ne permettent pas d'observer une telle évolution. L'approfondissement de cette question repose sur l'amélioration de la qualité des données recueillies par les registres qui actuellement ne recueillent pas systématiquement le stade des cancers. Ainsi, le pourcentage de données manquantes est, dans certains registres, trop important pour que l'on puisse conclure. Cependant, la tendance actuelle est le recueil de plus en plus systématique des stades de cancer. 4. Pour une évaluation nationale ou ciblée sur quelques départements ? Il apparaît que, début 2004, l'évaluation de l'efficacité du programme de dépistage est encore insuffisante en France. Toutefois, tous les dispositifs prévus par l'InVS ne sont pas encore opérationnels, en particulier les réseaux anatomocytopathologiques. Il ne paraît cependant pas réaliste d'envisager une évaluation approfondie de l'efficacité du programme de dépistage (avec étude systématique des cancers de l'intervalle, de la répartition des stades au diagnostic) sur l'ensemble du territoire. Il serait au contraire préférable de concentrer les efforts financiers et humains sur l'évaluation du programme de dépistage dans quelques départements au sein desquels les registres et/ou recueils de données seraient de grande qualité. Logiquement, ces départements sont à choisir parmi les départements possédant déjà un registre du cancer ou un recueil de données des cancers. Ce n'est que dans ces conditions de qualité optimale, que l'impact escompté du dépistage organisé pourra être mis en évidence. Pour les autres départements, au moins dans un premier temps, il serait suffisant de disposer des valeurs des principaux indicateurs de qualité et d'efficacité tels que le taux de participation et les taux de détection mesurés rigoureusement. Ce minimum n'est actuellement pas atteint. Une telle organisation permettrait d'avoir des indications générales sur l'ensemble du territoire tout en garantissant une évaluation approfondie de l'efficacité du programme de dépistage dans quelques départements représentatifs. 5. L'observatoire de sénologie L'avenant relatif à l'accord de bon usage des soins en mammographie publié en juillet 2003 prévoit la création d'un observatoire national de la pratique mammographique sous la responsabilité de la Fédération nationale des médecins radiologues (FNMR). L'objectif de cet observatoire est de recueillir des données sur la pratique libérale de tous les radiologues en matière de mammographie (motif d'examen, nature des actes et autres examens pratiqués..). Il devrait être pleinement opérationnel en juin 2004 et les premiers résultats devraient être publiés fin 2005. 5. Le recueil des données économiques L'InVS ne recueille pas d'information sur le coût du dépistage, cela est fait par les organismes d'assurance maladie mais ces données sont peu exploitées. Il est probable que le coût du dépistage varie d'un département à l'autre selon la formation des radiologues ou encore le pourcentage d'images considérées comme suspectes ayant fait l'objet d'examens complémentaires. De plus, on peut escompter que le coût diminuera avec l'expérience acquise mais probablement pas au même rythme dans tous les départements. Face à la mise en pratique du nouveau cahier des charges et aux nouvelles obligations en matière de contrôle de qualité, il est primordial de prévoir des études du coût du programme de dépistage dans un échantillon représentatif des départements français. Ces études permettront alors de disposer du rapport coût-efficacité pragmatique du programme de dépistage. 6. Le problème posé par le dépistage individuel La persistance d'un nombre significatif d'actes de dépistage individuel, échappant à toute évaluation, demeure un obstacle majeur à l'évaluation du programme national de dépistage organisé. En effet, dans les études d'impact du dépistage organisé, le groupe dépisté est, de ce fait, comparé à un groupe de femmes chez lesquelles les mammographies de dépistage sont relativement fréquentes et non pas à un groupe sans dépistage. Les différences observées sont donc réduites et plus difficiles à mettre en évidence. En conclusion, l'évaluation du programme de dépistage du cancer du sein est répartie entre différentes structures n'ayant pas toujours les moyens humains et financiers d'assurer cette responsabilité. Il en résulte la nécessité de réaliser des études ad hoc complémentaires. Dans l'état actuel de sa mise en place, il apparaît ainsi que l'évaluation du programme de dépistage du cancer du sein en France est actuellement le maillon faible du dispositif. Parmi l'ensemble des cancers du sein, environ à 7 à 10 % sont dus à une prédisposition génétique majeure. Les deux gènes les mieux connus actuellement et dont la mutation induit une prédisposition au cancer du sein sont les gènes BRCA1 et BRCA2 (pour BReast CAncer 1 et 2) mais il semble qu'ils ne permettent d'expliquer qu'une part modeste des formes familiales du cancer du sein (environ 20 %) [Bonadona and Lasset 2003]. Les cancers héréditaires apparaissent en moyenne plus précocement que les formes sporadiques, 43 ans versus 60 ans en moyenne (enquête INSERM) et leurs caractéristiques histologiques sont plus défavorables à la détection par mammographie [Lasset and Bonadona 2001]. 2. L'efficacité du dépistage par mammographie dans cette population Les données actuelles de la littérature ne comportent aucun essai permettant d'évaluer l'efficacité de la mammographie chez les femmes présentant un risque génétique de cancer du sein. Les études publiées montrent que la mammographie permet chez ces femmes de détecter des tumeurs de petite taille mais, étant donné qu'elles n'impliquent qu'un petit nombre de femmes, elles ne permettent pas de conclure quant à l'effet du dépistage par mammographie sur la mortalité par cancer du sein [Brekelmans 2001 ; Kollias 1998 ; Lalloo 1998]. Par ailleurs, dans deux d'entre elles, le taux de cancers de l'intervalle est très élevé (26 % après 3 ans de suivi dans l'étude de Brekelmans et 34 % après 22 mois de suivi dans l'étude de Kollias) ce qui laisse supposer que l'efficacité du dépistage mammographique est limitée. La sensibilité de la mammographie dans ces études est respectivement de 74 % et 79 % a donc tendance à être plus faible que dans la population générale. Une étude actuellement en cours au Royaume-Uni [Mackay 2001] a pour objectif de comparer, d'une part, une cohorte de 20 000 femmes âgées de 40 à 44 ans présentant des antécédents familiaux de cancer du sein à qui l'on propose une surveillance mammographique annuelle avec, d'autre part, un groupe contrôle de 106 000 femmes à risque génétique âgées de 40 à 41 ans au moment du recrutement suivies pendant 10 ans et qui ne seront pas dépistées pendant cette période. Même si cette étude n'est pas un essai randomisé, elle devrait permettre de mieux appréhender l'impact d'une surveillance mammographique chez les femmes à risque génétique de cancer du sein en particulier sur la mortalité par cancer du sein. Les résultats sont attendus pour 2006-2007. Cette étude prévoit également une estimation du rapport coût-efficacité du dépistage dans cette population. Par ailleurs, il serait intéressant de prévoir en France une évaluation des pratiques actuelles en matières de dépistage dans cette population. Une possibilité serait d'exploiter les données recueillies au niveau de l'observatoire de sénologie qui sera mis en place par la FNMR. En effet, cet observatoire prévoit de recueillir pour chaque mammographie effectuée le risque familial connu. 3. Les modalités actuelles de dépistage chez les femmes à risque génétique Les recommandations actuelles en France pour les femmes à risque génétique sont issues de l'expertise collective INSERM-FNCLCC datant de 1998 [Eisinger 1999] et dont la mise à jour sera très prochainement publiée dans le Bulletin du Cancer. Face aux manques de données, ces recommandations sont le résultat d'un consensus d'experts basé sur l'analyse de la littérature et sur les connaissances actuelles des cancers du sein héréditaires. Ces recommandations concernent les femmes ayant un risque de plus de 25 % d'avoir un gène de prédisposition muté et sont les suivantes : - une mammographie annuelle à deux incidences à partir de l'âge de 30 ans (ou 5 ans avant l'âge du cancer du sein le plus précoce dans la famille) ; - double lecture systématique ; - 1 à 2 examens cliniques par an. Les mammographies effectuées dans ce cadre sont soumises aux mêmes exigences de qualité que celles des mammographies effectuées dans le cadre du programme de dépistage organisé. Enfin, cette surveillance doit s'accompagner d'une information auprès des femmes sur les avantages potentiels d'un dépistage régulier et sur les limites de cette stratégie. En particulier, la mammographie ne permettant pas de détecter 100 % des tumeurs, les femmes doivent rester vigilantes à l'apparition de symptômes même peu de temps après une mammographie normale. Il est à noter que l'expertise collective FNCLCC-INSERM propose une deuxième stratégie de prévention possible pour les femmes à risque génétique à savoir la chirurgie prophylactique qui permet de réduire le risque de survenue de cancer. Cette stratégie ne peut être indiquée que dans des conditions très particulières. L'évaluation de l'utilisation de la mammographie chez les femmes à risque génétique de cancer du sein est actuellement très succincte. Par ailleurs, plusieurs études suggèrent que la sensibilité de la mammographie est moins bonne chez ces femmes que dans la population générale [Huo 2002] et en particulier chez les femmes porteuses d'une mutation sur BRCA1 ou BRCA2 [Brekelmans 2001]. Actuellement, l'utilisation d'autres techniques est en cours d'évaluation. Celles qui paraîtraient appropriées sont les examens d'imagerie plus performants en cas de densité mammaire importante comme l'échographie ou l'imagerie à résonance magnétique (IRM). La sensibilité de cette dernière est de l'ordre de 90 à 100 % [Kuhl 2000 ; Warner 2001] chez les femmes à risque génétique. Des études sur de plus grands effectifs et avec une durée de suivi plus longue sont nécessaires pour confirmer ce résultat et pour mieux étudier si les taux de faux positifs et de faux négatifs associés à l'IRM sont compatibles avec l'utilisation de cette technique en routine. Certaines sont en cours notamment l'étude MARIBS au Royaume-Uni, [Leach 2002]. Par ailleurs, l'utilisation de la mammographie numérique chez ces femmes fait également objet de débat en attente en particulier des résultats de l'étude DMIST. La mise à jour des recommandations de l'expertise collective FNCLCC/INSERM propose d'ores et déjà que l'utilisation des systèmes numériques puisse être envisagée chez les femmes à risque génétique de cancer du sein sachant, en particulier, que la dose d'exposition aux rayons X utilisée pour ces systèmes est plus faible qu'en mammographie conventionnelle. Le dernier rapport de l'InVS donne les résultats du programme de dépistage au 31 décembre 2000 et concerne les trente-deux premiers départements alors engagés dans la démarche [Institut national de veille sanitaire 2000]. Ces départements regroupent environ 45 % de la population française âgée de 50 à 69 ans. Les valeurs des indicateurs pour l'année 2000 sont regroupées dans le tableau 4. Quelques-unes de ces valeurs sont commentées ci-dessous. Le rapport de l'InVS contenant uniquement des données moyennes ou des données par départements mais restant anonymes (sans préciser le nom des départements), nous avons cherché à nominaliser les valeurs par départements de ces indicateurs. Malheureusement, ces indications ne nous ont pas été fournies par l'InVS. Toutefois, le cahier des charges de 2001 prévoit une publication nominative des résultats départementaux, ce devrait donc être le cas pour les données de 2002. Les taux en prévalence correspondent à la première vague de mammographies effectuées dans le cadre du programme au sein d'un département. Les taux en incidence correspondent aux vagues suivantes. Tableau 4 : indicateurs du programme de dépistage organisé pour l'année 2000 (données InVS, rapport 31 décembre 2000) *
* A cette date, 32 départements avaient mis en place le programme de dépistage. Pour ces valeurs, la durée de la campagne a été prise en compte pour chaque département. Sont indiquées également les valeurs de référence de ces indicateurs données par la Commission européenne. Les valeurs en prévalence correspondent aux premières mammographies et les valeurs en incidence aux mammographies suivantes. Taux de participation En 2000, 478 751 mammographies ont été réalisées dans le cadre du programme de dépistage ce qui signifie que globalement 38,3 % des femmes invitées ont participé. Cette moyenne est insuffisante (selon les recommandations européennes, le taux ciblé est d'au moins 70 %) et masque des disparités importantes entre les départements (variation de 20 à 60 %). Cependant, on observe qu'à l'échelle d'un département, le taux de participation s'améliore au cours du temps dans la plupart des cas. Le taux de 38,3 % de participation recouvre aussi bien les premières mammographies réalisées dans le cadre du dépistage organisé que les suivantes. Sur l'ensemble des mammographies réalisées en 2000, 47 % correspondaient à une première mammographie. Or la donnée pertinente pour les résultats à long terme du programme de dépistage est la proportion de femmes participant régulièrement au dépistage. Cette donnée peut être estimée par les taux de fidélisation (tableau 5). Ceux-ci sont faibles. Ils font ressortir que peu de femmes répondent à des invitations successives. Or la réduction sur la mortalité ne sera perceptible que si la participation des femmes est importante dans la durée. Par ailleurs, ces données montrent que la participation d'une femme à une mammographie une année donnée augmente peu la probabilité qu'elle participe deux ans après. Ceci suggère que l'on ne peut pas réellement distinguer une population de femmes participant au dépistage d'une autre ne participant pas. Cependant, ces chiffres ne reflètent pas la couverture réelle du dépistage puisqu'en parallèle du dépistage organisé existe en France un important dépistage « spontané » qui est pratiqué dans le cadre du fonctionnement en routine du système de soins. Selon le baromètre de la santé du CFES, en 2000, 55,6 % des femmes de la tranche d'âge 50-69 ans avaient bénéficié d'une mammographie au cours des deux dernières années précédant l'enquête. Nous n'avons actuellement que très peu d'information sur ce dépistage « spontané » et en particulier sur sa fréquence. En conclusion, le taux de couverture du dépistage organisé doit s'améliorer impérativement dans les 5 ans. Cette amélioration devrait constituer un paramètre clé pour le renouvellement ou non du programme de dépistage organisé à l'avenir. Tableau 5 : taux de fidélisation des femmes Selon les taux de fidélisation de l'année 2000 Sur 100 femmes Taux de fidélisation 46 % 46 femmes 
Taux de fidélisation 40 % 8 femmes  3 femmes Taux de rappel Parmi les anomalies détectées lors de la mammographie, beaucoup n'ont pas de signification médicale et ne nécessitent pas la réalisation d'examens complémentaires. A l'inverse, certaines conduisent à la réalisation d'une échographie voire d'une microbiopsie pour préciser le diagnostic. Le taux de ce deuxième type d'anomalies est le reflet de l'équilibre entre sensibilité et spécificité du test. Selon les recommandations européennes, il doit être au maximum de 7 % en prévalence et au maximum de 5 % en incidence. Au-delà de ces valeurs, le taux de faux positifs est à un niveau qui doit être considéré comme trop élevé pour la population générale. Au contraire, si ce taux est très bas, cela peut refléter un taux de faux négatifs trop élevé. En 2000, ce taux correspondait bien pour le programme français à ces recommandations puisqu'il était en moyenne de 7,7 % en prévalence et de 4,8 % en incidence. Taux de cancers détectés Parmi les anomalies détectées, les analyses anatomocytopathologiques permettent de définir celles qui sont au stade tumoral. Pour un programme de dépistage efficace, le taux de cancer diagnostiqué doit être au moins de 5 0/00 en prévalence et de 3 0/00 en incidence. Il est plus faible chez les femmes suivies régulièrement par mammographie. En 2000, dans le programme français, il était en moyenne de 5,2 0/00 en prévalence et de 4,1 0/00 en incidence. Valeur prédictive de la biopsie Cet indicateur indique le pourcentage de femmes réellement atteintes d'un cancer parmi celles ayant subi une biopsie chirurgicale. Selon les recommandations européennes de 2001, ce taux doit être supérieur à 50 % (en incidence et en prévalence) [Ancelle-Park 2003]. Cela signifie que l'on tolère encore qu'une femme sur deux subissant une biopsie chirurgicale ne soit pas réellement atteinte d'un cancer. Ce taux de référence peut néanmoins être considéré comme trop faible. Les résultats varient beaucoup d'un département à l'autre selon les performances des équipes d'anatomopathologie. En 2000, ce taux avait une moyenne de 56,8 % en prévalence et de 68,1 % en incidence. Dans la plupart des départements, ces taux s'améliorent au cours du temps surtout lorsque se développe en parallèle l'accès au mammotome. De plus, ces taux sont plus élevés lorsque l'âge des femmes augmente. Taux de cancers invasifs et de taille inférieure ou égale à 10 mm Ce taux correspond à la proportion de cancers invasifs de taille inférieure ou égale à 10 mm parmi tous les cancers invasifs détectés. Ces cancers sont dits de « bon pronostic » et doivent être en proportion élevée dans le cadre du dépistage (au moins 20 % en prévalence et 25 % en incidence). En 2000, il était en moyenne de 33 % sur l'ensemble des départements. Cette proportion très élevée en France reflète probablement le fait qu'avant d'entrer dans le programme de dépistage, beaucoup de femmes ont déjà effectué une ou plusieurs mammographies. Taux de cancers in situ Ce taux concerne les carcinomes canalaires in situ. Ce type de cancer est plus fréquent chez les femmes jeunes. Les connaissances actuelles sur l'histoire naturelle de ces cancers ne permettent pas de différencier ceux qui évolueront vers un stade invasif de ceux qui n'évolueront pas. Dans le doute tous ces cancers sont actuellement traités. Selon les recommandations européennes, leur taux doit se situer entre 10 et 20 % (compromis entre une détection suffisante et un taux de faux positifs acceptable). Il était en moyenne de 15,5 % en 2000. Taux de femmes perdues de vue Selon un questionnaire InVS sur la campagne de 2000, 3,6 % des femmes chez qui une anomalie avait été détectée lors du dépistage ont été perdues de vue par la structure de gestion après la dernière mammographie. Ce suivi par la structure de gestion a pour objectif de vérifier que la femme entre dans une filière de soins et d'obtenir les informations sur le type de lésion diagnostiquée. Délai de prise en charge Les résultats dont on dispose concernent vingt-six départements. Le délai moyen de prise en charge, c'est-à-dire le délai moyen entre la date du dépistage et la date du premier traitement en cas de diagnostic de cancer, est de 2,6 mois et la médiane de 2 mois. Même si l'on soustrait à ces valeurs les 15 jours nécessaires à la double lecture, ce point est à améliorer d'une façon générale pour atteindre les recommandations européennes qui sont de 4 semaines au plus. Cette question sera approfondie par l'InVS pour tenter d'expliquer ces délais importants. En particulier, les délais moyens semblent être augmentés par les cas de femmes mises sous surveillance après la mammographie de dépistage et dont le traitement ne débute éventuellement que 6 à 12 mois plus tard. Conclusion Hormis les taux de participation et surtout de fidélisation, les indicateurs pour l'année 2000 du programme organisé de dépistage français sont conformes aux recommandations européennes même s'ils font apparaître des disparités importantes entre les départements. Face à cette situation, le dernier cahier des charges (2001), en cours d'application a comme objectif numéro un l'augmentation du taux de participation. L'évaluation de ce nouveau cahier des charges ne sera disponible qu'à la fin de l'année 2004. Depuis le début de la mise en place du programme de dépistage, 11 867 cancers ont été détectés dans le cadre de ce programme dont 2 216 en 2000. Pour l'année 2000, cela correspond à 5 % des nouveaux cas de cancers enregistrés sur l'ensemble du territoire [Institut national de veille sanitaire ; Remontet 2003]. Dans l'état actuel de la mise en place du programme de dépistage, l'impact du dépistage organisé, au niveau national, sur la mortalité par cancer du sein ne peut donc être que limité voire imperceptible. Alors que l'incidence du cancer du sein est en forte augmentation (21 211 nouveaux cas en 1980 et 41 845 en 2000 [Remontet 2003]), le taux de mortalité par cancer du sein est relativement stable au niveau national entre ces deux dates (18,7/100 000 personnes année en 1980 et 19,7/100 000 en 2000). L'amélioration des traitements pendant cette période est certainement un facteur majeur dans la stabilité de ce taux de mortalité alors que l'impact spécifique de la mise en place du programme de dépistage organisé est difficile à évaluer. Cette question mérite des études approfondies. En effet, il est essentiel de comprendre pourquoi le taux de mortalité par cancer du sein reste stable en France alors qu'il est en forte diminution dans d'autres pays tels que la Suède ou le Royaume-Uni. Est-ce dû à une qualité insuffisante du dépistage ? A un retard dans la généralisation du dépistage ? A une forte augmentation du nombre de cancers invasifs ? Pour étudier l'impact du dépistage organisé du cancer du sein, il faut disposer de données exhaustives sur la mortalité par cancer du sein à la fois chez les femmes participant au programme de dépistage et chez les femmes n'y participant pas. Ces données sont partiellement présentes dans les registres de cancer et n'ont de sens que 10 à 15 ans après le début de la mise en place du programme de dépistage. L'InVS met actuellement en place un groupe de travail dont l'objectif sera d'étudier l'impact à long terme du programme de dépistage sur la mortalité par cancer du sein. Une étude préliminaire, publiée par l'InVS, compare la mortalité par cancer du sein dans les départements ayant mis en place des programmes de dépistage depuis au moins 10 ans avec celle des autres départements. Entre ces deux groupes, une réduction significative moyenne de 7,7 % de la mortalité par cancer du sein a été mise en évidence [Ancelle-Park 2003] dans le groupe des départements ayant un programme de dépistage ancien. Cette réduction est essentiellement due à quatre de ces départements. Elle est encourageante même s'il est encore prématuré d'attribuer cette différence à la mise en place du programme de dépistage. Par ailleurs, pour ce type d'étude, il est essentiel de prendre en compte des différences inter-départementales au niveau des taux de mortalité par cancer du sein et au niveau de l'évolution de ces derniers dans le temps. Le fait qu'en France, comme nous l'avons signalé plus haut, les résultats du programme de dépistage ne sont pas comparés à une situation sans dépistage mais à une situation où le dépistage individuel est fréquent, atténue d'autant l'impact visible du dépistage organisé. C. LES FACTEURS INFLUENÇANT LA PARTICIPATION DES FEMMES AU PROGRAMME DE DÉPISTAGE ET L'INFORMATION DÉLIVRÉE AUX FEMMES 1. Les motifs de non-participation des femmes Un des principaux points faibles de la mise en place du programme de dépistage en France est la faiblesse du taux de participation. Cette non-participation recouvre à la fois des femmes qui sont dépistées dans le cadre du fonctionnement de routine du système de soins (dépistage « spontané ») et des femmes qui ne sont pas dépistées. Plusieurs facteurs sont corrélés avec ces deux types de comportement. Il a été montré en particulier par l'Observatoire régional de la santé de la région Provence-Alpes-Côte d'Azur qu'il existe une corrélation significative entre le taux de chômage et la mortalité par cancer du sein. Ce travail montre que cette corrélation est le reflet d'une inégalité au niveau de l'accès au dépistage et non au niveau de l'accès aux soins. Dans un milieu socio-économique défavorisé et / ou dans un contexte de moindre éducation, les femmes sont globalement éloignées de tout dispositif de prévention et a fortiori du dépistage systématique du cancer du sein. D'après une étude réalisée par le Collège Rhône-Alpes d'éducation pour la santé et le Centre régional d'information et de prévention du sida (CRAES-CRIPS) auprès de femmes en situation de précarité, leurs principales raisons de non-participation sont : le fait que les messages de prévention sont en décalage avec leurs conditions de vie et leurs préoccupations quotidiennes, la non-compréhension des brochures et de l'intérêt du dépistage, la peur de se faire dépister et les obstacles pratiques pour se rendre au rendez-vous de mammographie. Au niveau national, il serait possible d'avoir une meilleure estimation de l'influence du niveau socio-économique sur la participation du dépistage en analysant notamment le taux de femmes bénéficiant de la couverture maladie universelle et participant au programme de dépistage organisé. Cette analyse est techniquement possible à partir des données de la CNAMTS, mais nécessite un délai important et nous n'avons pas pu l'obtenir dans les délais impartis. L'InVS travaille actuellement sur ce sujet. A l'opposé, parmi les femmes qui ne participent pas aux campagnes de dépistage certaines le font par choix. Selon une enquête réalisée en 1998 par l'association Recherches et évaluations sociologiques sur le social, la santé et les actions communautaires (RESSCOM) à la demande de la DGS et de la Ligue nationale contre le cancer, surtout chez les femmes de milieux sociaux favorisés, le programme de dépistage organisé peut être associé à une image de médecine de masse de moindre qualité, et réservée aux populations défavorisées. Au contraire, le dépistage individuel prescrit pas leur gynécologue habituel est beaucoup mieux accepté [Ancelle-Park 2003] même s'il n'intègre pas, en pratique, toutes les procédures d'assurance qualité. L'examen de la littérature internationale montre que la participation à un programme de dépistage du cancer du sein est influencée par d'autres facteurs que le milieu socio-économique. En particulier, la relation avec le monde médical en général et le médecin traitant en particulier est essentielle. D'une part, la fréquence des contacts avec le système de soins (nombre de consultations annuelles avec un généraliste et / ou un gynécologue) est liée à la participation au dépistage [Barr 2001 ; Chamot and Perneger 2003]. D'autre part, le discours du médecin sur le dépistage est un élément clé de la participation des femmes [Chamot and Perneger 2003 ; Lauver 2003]. Dans l'étude de l'association RESSCOM déjà citée, les femmes interrogées soulignent que les médecins généralistes sont rarement associés au processus de dépistage et ont souvent un discours qui les dissuade de participer [Ancelle-Park 2003]. Enfin, une expérience personnelle antérieure négative vis-à-vis de la médecine peut décourager les femmes à participer au programme de dépistage organisé, dispositif fortement médicalisé [Ancelle-Park 2003]. La perception individuelle du risque de cancer (moyenne ou forte), l'habitat en milieu rural, la mise en place d'un programme de dépistage organisé dans la région d'habitation, ainsi que le style de vie général sont également des facteurs influençant la participation des femmes [Maxwell 2001]. Enfin, différentes études montrent que le taux de participation des femmes a tendance à diminuer avec l'âge. Les données de 2000 de l'InVS indiquent néanmoins que le taux de participation le plus important est observé chez les femmes âgées de 65 à 69 ans [Institut national de veille sanitaire 2000]. Les facteurs décrits ci-dessus qui influencent la participation, qu'ils soient sociaux ou psychologiques, peuvent varier au cours de la vie d'une femme. Comme le suggèrent les taux de fidélisation calculés par l'InVS, la motivation d'une femme à participer au programme de dépistage est donc susceptible d'évoluer sensiblement avec le temps. Il est donc important d'en tenir compte pour renouveler et adapter régulièrement les messages d'incitation à la participation au dépistage. L'abandon du dépistage après une première expérience est observé chez un trop grand nombre de femmes ce qui est très préjudiciable à l'efficacité du programme de dépistage. L'information auprès des femmes devrait plus insister sur la nécessité de pratiquer régulièrement (tous les deux ans) et à long terme une mammographie de dépistage. Plus globalement, la stratégie de communication pour favoriser la participation au programme de dépistage doit être repensée. En effet, les campagnes classiques menées jusqu'à présent ont montré les limites de leur efficacité. Un groupe de travail pluridisciplinaire GRESAC / ADEMAS 69 doit produire un rapport sur ce sujet et se propose d'aborder scientifiquement cette question. 2. Exemples d'actions ciblées vers les populations exclues du dépistage Plusieurs types d'actions ciblées à destination des populations défavorisées et/ou exclues du dépistage ont déjà prouvé leur efficacité. L'expérience des mammographes mobiles (mammobiles) a montré que ce moyen permet d'atteindre efficacement des populations isolées ou pour lesquelles un déplacement est un obstacle majeur. Les résultats obtenus à ce sujet dans le département de l'Aveyron sont très encourageants puisqu'un an après le lancement du programme, 30 % des femmes reçues au mammobile n'avaient jamais fait de mammographie de dépistage auparavant (APM Reuter Santé 2002). De même, les programmes soutenus en parallèle par des interventions socio-culturelles ciblées ont montré leur efficacité. Plusieurs départements ont édité des brochures simplifiées à destination des populations défavorisées, le plus souvent dans plusieurs langues. L'utilisation d'autres médias d'informations telles que les radios locales ou la presse locale permet d'atteindre une population plus large. Enfin, l'information, sous forme orale ou écrite, passe également dans certains départements par les pharmacies, les travailleurs sociaux ou encore les structures d'alphabétisation. Ce type de démarche doit être fortement encouragé et généralisé à tous les départements. Il a été souligné l'intérêt d'associer l'information sur le dépistage du cancer du sein à une sensibilisation plus globale des femmes à la prise en charge de leur santé. Cette expérience est actuellement menée dans la région Provence-Alpes-Côte d'Azur. On retrouve par ailleurs cette demande de la part des femmes elles-mêmes : dans l'étude CRAES-CRIPS celles-ci souhaiteraient le développement du nombre «d'accompagnateurs santé » avec lequel elles pourraient dialoguer et qui les aideraient et les rassureraient dans toutes leurs démarches vers le système de santé. 3. L'importance de la qualité de l'information L'objectif d'augmenter le taux de participation ne doit pas se faire au détriment de la qualité de l'information fournie. Certains documents publiés trop simplificateurs fournissent une information biaisée où il est sous-entendu que dépister un cancer s'accompagne toujours de la guérison de celui-ci (exemple : « Grâce à cet examen, le cancer est pris à temps et l'on guérit plus vite, plus facilement »). Il est pourtant essentiel que l'information soit complète et décrive non seulement les avantages du dépistage mais également ses limites (faux négatifs, cancers de l'intervalle, faux positifs). C'est à cette seule condition que les femmes pourront choisir librement de participer ou non au programme de dépistage. Ces considérations ne sont pas uniquement d'ordre éthique mais répondent aux impératifs fixés par la loi du 4 mars 2002 relative aux droits des malades et à la qualité du système de santé selon laquelle toute personne a droit d'être informée sur les actions de prévention qui lui sont proposées, sur leur utilité, leurs conséquences et sur les risques qu'elles comportent. Une équipe anglaise vient de développer un modèle pour présenter le devenir prévisible d'un groupe de 1 000 femmes (survie, biopsies) selon qu'elles participent ou non au dépistage organisé qui a l'avantage de pouvoir être présenté sous forme de schémas simples [Marshall and Adab 2003]. Ce modèle qui reste à être évalué sur un échantillon de femmes devrait permettre aux femmes d'avoir des attentes plus réalistes au sujet de l'efficacité du dépistage. Par ailleurs, une meilleure information devrait également leur permettre de mieux comprendre les résultats des mammographies qui sont parfois présentés abusivement de manière dichotomique « cancer » ou « pas de cancer » [Goyder 2000]. La qualité de l'information repose aussi sur son adéquation à la population ciblée. L'information doit être adaptée à l'âge des femmes, au milieu socio-économique et aux habitudes culturelles des femmes à qui elle est destinée. Enfin, il est important que les médecins (généralistes ou gynécologues) en tant que médiateurs privilégiés de l'information délivrée aux femmes participent activement à l'amélioration de la qualité de cette information. Certains documents de la campagne « Rendez-vous santé plus » leur sont particulièrement destinés dans ce but. Très peu d'études ont été publiées en France sur l'évaluation économique du programme de dépistage organisé du cancer du sein. Seuls trois départements disposent de telles données : Le Bas-Rhin, les Bouches-du-Rhône et l'Hérault. L'organisation du programme de dépistage en France est décentralisée et, de ce fait est plus coûteuse que dans un système centralisé [Wait 2000]. Selon l'étude de Van Ineveld et al., les coûts seraient augmentés d'environ 60 % dans un système décentralisé par rapport à un système centralisé [Van Ineveld 993]. Néanmoins, selon les données dont on dispose, la mise en place du programme de dépistage organisé du cancer du sein reste un dispositif efficient de santé publique. Le coût par année de vie gagnée est de l'ordre de 10 000 à 20 000 euros [Arveux 2003, Daurès 1998]. Cette évaluation devrait être mise à jour pour tenir compte des nouvelles modalités de mise en place du programme de dépistage. Quelques études sont en cours ou en projet en particulier en Ile-de-France et dans les Bouches-du-Rhône. L'augmentation visée du taux de participation pour les années à venir pourrait avoir tendance à améliorer le rapport coût-efficacité du programme. Toutefois, cet effet sera limité étant donné que selon S. Wait [Wait 2000] les coûts fixes ne représentent qu'une part modeste des coûts moyens par femme participante (20-30 %). La mise en œuvre décentralisée du programme de dépistage est associée en France au grand nombre d'installations de mammographie existantes. Paradoxalement, la large diffusion des équipements de mammographie est l'un des facteurs qui a pu expliquer les retards dans la généralisation de la mise en place d'un programme organisé et standardisé à l'ensemble du territoire. Les retombées de la mise en œuvre du programme de dépistage organisé s'avèrent cependant d'ores et déjà tout à fait positives et dépassent largement le cadre du dépistage du cancer du sein proprement dit. En effet, cette expérience contribue à diffuser en médecine libérale de ville les notions d'assurance de qualité, d'évaluation des résultats obtenus, de formation continue ainsi que de travail en réseau. Elle pose les bases de la mise en place de politique de santé publique en médecine libérale et sera probablement une référence dans la mise en place de programmes de dépistage futurs pour d'autres cancers, voire d'autres pathologies. 1. Les femmes âgées de 40 à 49 ans Les recommandations de l'ANAES de 1999 ne recommandaient pas la mise en place du dépistage systématique chez les femmes âgées de 40 à 49 ans. En effet, chez ces femmes, l'incidence du cancer du sein est plus faible qu'à un âge plus avancé et la sensibilité de la mammographie est moins bonne chez les femmes jeunes. De plus, les résultats des essais internationaux ne permettent pas de mettre en évidence une réduction significative de la mortalité par cancer du sein grâce au dépistage systématique dans cette tranche d'âge. Une actualisation de ce point est en cours à l'ANAES (« Opportunité d'étendre le programme national de dépistage du cancer du sein aux femmes âgées de 40 à 49 ans »), sa publication est prévue pour le milieu de l'année 2004. 2. Les femmes âgées de 70 ans ou plus Selon les données issues des registres du cancer, l'incidence du cancer du sein augmente régulièrement avec l'âge avec une rupture de pente au moment de la ménopause. Par ailleurs, l'évolution démographique tend vers une augmentation de l'effectif de la population féminine âgée de plus de 70 ans. Ces deux éléments posent la question de l'opportunité d'étendre le dépistage systématique du cancer du sein au-delà de 70 ans. Les données de la littérature concernant cette tranche d'âge sont très insuffisantes et peu fiables. En effet, parmi les essais expérimentaux, seuls les essais Kopparberg et Östergland prévoyaient d'inclure des femmes âgées de plus de 70 ans. Or, après 20 ans de suivi, aucune réduction significative de la mortalité par cancer du sein n'a pu être mise en évidence chez les femmes âgées de 70 à 74 ans [International Agency for Research on Cancer 2002]. Il est vrai que, chez ces dernières, les taux d'observance au cours des études étaient très faibles (environ 20 %). Une récente étude de cohorte réalisée en Suède montre une réduction non significative de la mortalité par cancer du sein chez les femmes de 70-74 ans invitées à un dépistage régulier par rapport à celles qui ne le sont pas [Jonsson 2003]. Ces auteurs soulignent la difficulté d'étudier le critère mortalité par cancer du sein chez des femmes chez qui les pathologies concomitantes sont particulièrement fréquentes. En l'absence de résultats plus précis, plusieurs équipes ont tenté de modéliser l'extension du dépistage du cancer du sein aux femmes de plus de 70 ans en tenant compte notamment de l'augmentation avec l'âge de la sensibilité de la mammographie et de sa valeur prédictive positive, de l'espérance de vie des femmes et d'un possible ralentissement du développement des tumeurs du sein chez les femmes plus âgées. En prenant également en compte les modélisations du rapport coût-efficacité, il apparaît que l'équilibre bénéfice / risque ne serait pas favorable à la généralisation du dépistage chez ces femmes [Zappa 2003]. Pour ces auteurs, la question de la poursuite du dépistage au-delà de 70 ans doit se poser au cas par cas. Il pourrait être justifié de la proposer aux femmes sans pathologie concomitante grave, qui se considèrent comme étant en bonne santé et qui ne sont pas trop anxieuses face aux inconvénients du dépistage [Barratt 2002 ; Zappa 2003]. Chez celles-ci, les bénéfices du dépistage devraient rester supérieurs à ses effets potentiellement négatifs. Dans ce type de scénario, le choix du dépistage doit être fait par la femme en concertation avec l'équipe médicale sur la base d'une information de qualité. Pour d'autres auteurs, il est urgent de généraliser le dépistage du cancer du sein chez les femmes âgées de plus de 70 ans en France [Hill 2004]. En effet, ces femmes sont peu surveillées en matière de dépistage du cancer du sein et la décroissance de l'incidence du cancer du sein à partir de la tranche d'âges 75-80 ans, non observée dans d'autres pays, serait en réalité le reflet d'un sous-diagnostic des tumeurs mammaires. Pour trancher entre ces différentes hypothèses et comme l'indique la récente méta-analyse de Mandelblatt [Mandelblatt 2003], il est nécessaire que soient menées des études évaluant spécifiquement l'impact du dépistage chez les femmes de plus de 70 ans en tenant compte de l'hétérogénéité de l'état de santé des femmes à partir de cet âge. Ces études devraient également préciser la périodicité avec laquelle le dépistage serait justifié chez ces femmes. En conclusion, dans l'état actuel des connaissances, il est plus raisonnable de concentrer les efforts en matière de dépistage en direction de la tranche d'âges (50-69 ans) pour laquelle l'efficience du dépistage du cancer du sein a été montrée. Pour les femmes plus jeunes, le dépistage régulier n'est justifié que dans certains cas particuliers (femmes à risque, suivi de l'évolution d'une anomalie bénigne...). Pour les femmes plus âgées, il est nécessaire de faire rapidement des études complémentaires pour éclaircir ce point. La poursuite du dépistage jusqu'à 74 ans (politique française actuelle) apparaît comme une position raisonnable dans l'attente d'études plus détaillées sur cette question. L'accord de bon usage des soins limitera, à partir du janvier 2006, la réalisation des mammographies aux radiologues effectuant personnellement au moins 500 mammographies par an et des incitations financières sont prévues pour supprimer les sites de faible activité mammographique. Toutefois, un radiologue pourra atteindre le chiffre de 500 mammographies par an en réalisant des doubles lectures en doublon lorsque les conditions démographiques le justifient. Nous n'avons pas pu obtenir, y compris auprès de la Fédération nationale des médecins radiologues (FNMR), d'estimation de la réduction possible du nombre de radiologues pratiquant la mammographie faisant suite à cette condition. Par ailleurs, l'accessibilité au dépistage est soumise à l'évolution de la démographie médicale. Les modèles d'évolution de la démographie médicale prévoient une réduction du nombre de médecins plus ou moins prononcée selon les spécialités [Niel 2002]. Ces modèles sont basés sur l'hypothèse du maintien du numerus clausus et des places de spécialités au concours d'internat. En ce qui concerne les radiologues-radiothérapeutes, la réduction prévue est de 7,7 % entre 2001 et 2010 et de 32 % entre 2001 et 2020. Cette forte réduction est à relativiser étant donné la forte augmentation entre 1984 et 2001 qui l'a précédé (+ 53 %). Cependant, si ces réductions peuvent être atténuées par des mesures telles que l'augmentation du numerus clausus ou la réorganisation du cursus médical, cette évolution est à prendre en compte pour la mise en œuvre à venir du programme de dépistage organisé. Le déficit en radiologues sera d'autant plus sensible si l'augmentation visée de la participation des femmes au programme de dépistage a lieu. Il est donc indispensable d'anticiper dès maintenant cette augmentation prévisible du nombre annuel de mammographie et de proposer des solutions efficaces pour éviter des délais de rendez-vous pour mammographie trop importants. En effet, si l'on vise une participation de 70 % de la tranche d'âge 50-74 ans, cela correspond à environ 2 700 000 mammographies par an dans le cadre du dépistage organisé soit 5,6 fois plus que le nombre réalisé en 2000 dans ce cadre. Sur la base des 3000 mammographes en fonction actuellement, cela correspond à environ 900 mammographies de dépistage par mammographe et par an. Face à cette question, une des solutions pourrait être l'utilisation d'outil d'aide à la décision lors de la lecture des mammographies, offrant un gain de temps non négligeable aux radiologues (communication personnelle de M. Zighed). Même si le cahier des charges actuel du programme de dépistage dispense les femmes d'avoir une ordonnance médicale pour participer (les invitations sont envoyées directement par la structure de gestion), nous avons souligné précédemment l'importance du rôle du médecin dans la participation des femmes au dépistage. Or la réduction prévue de l'effectif des gynécologues, est de 5 % entre 2001 et 2010 et de 27 % entre 2001 et 2020. En parallèle, la réduction prévue des effectifs de médecins généralistes est respectivement de 1 % et 11 %. Ces chiffres montrent qu'il est d'autant plus important de sensibiliser dès maintenant les médecins généralistes au programme de dépistage du cancer du sein afin qu'ils suppléent, dans les années à venir, le déficit potentiel de gynécologues pour diriger les femmes vers le dépistage. Les chiffres cités correspondent à des moyennes nationales et ne reflètent pas les disparités de la démographie médicale entre les régions. Il est fort probable si aucune mesure n'est prise, que les difficultés d'accès au dépistage risquent d'être critiques surtout dans les zones déjà pauvres en médecins telles que les zones rurales ou périurbaines. Ce problème n'est pas spécifique du dépistage du cancer du sein. Les tendances qui viennent d'être soulignées sont des éléments clés de l'équilibre difficile entre accessibilité et qualité du dépistage. Des solutions doivent être imaginées dès maintenant pour pouvoir garantir à long terme un accès au dépistage à toutes les femmes du territoire avec des délais de rendez-vous raisonnables. En particulier, les solutions pratiques telles que l'utilisation de mammobiles ou l'organisation du transport remboursé vers les centres de radiologie ne sont pas à négliger. Par ailleurs, il sera peut-être nécessaire de prévoir des exceptions à accorder ponctuellement à des radiologues n'atteignant pas les 500 mammographies par an en pratique courante pour maintenir un site de dépistage. Dans ces conditions, on peut imaginer que les clichés seraient systématiquement soumis à une double lecture. Selon la note du 3 novembre 2003 de la DHOS et de la DGS, les établissements hospitaliers qui ont vocation à s'engager dans la démarche du programme de dépistage organisé du cancer du sein sont ceux qui 1) comblent un besoin de proximité non couvert par la radiologie libérale et/ou 2) ont déjà une activité mammographique importante ouverte sur l'extérieur et/ou 3) offrent une prise en charge sénologique complète. D'une façon générale, l'activité mammographique des grands établissements hospitaliers est essentiellement de type diagnostique et pour ces structures, la limite de 500 mammographies par an et par radiologue pourrait se poser en d'autres termes que pour les radiologues de ville. En effet, parmi les femmes consultant dans les grands centres hospitaliers, la majorité correspond à des cas de diagnostic difficile. Par ailleurs, le travail en équipe favorise les échanges sur les cas litigieux et la formation continue des médecins. Cette situation particulière permet aux radiologues des CHU (centres hospitaliers universitaires) et des CRLCC (centres régionaux de lutte de contre le cancer) d'acquérir une expertise reconnue par l'ensemble de la profession. Si l'avancée que constitue la démarche qualité mise en place dans le programme national de dépistage n'est bien sûr en aucun cas remise en cause par les radiologues des grandes structures hospitalières, ces deniers persistent dans leur demande expresse qu'elle soit adaptée à l'activité spécifique des centres hospitaliers. Actuellement, les textes législatifs, conçus pour le système libéral, ne sont, selon eux, pas adaptés à cette situation puisqu'ils ne prévoient pas de différences entre un radiologue hospitalier et un radiologue de ville quant aux conditions de participation au dépistage organisé. Cette analyse n'est pas partagée par l'ensemble des experts ayant participé à ce travail. Les radiologues libéraux notamment considèrent que le seuil des 500 mammographies par an est suffisamment bas et qu'il ne doit pas être remis en cause. La note du 3 novembre 2003 de la DHOS/DGS prévoit le cas particulier des internes en radiologie, qui doivent effectuer les actes mammographiques en doublon d'un senior, mais n'envisage pas le cas des radiologues vacataires. Ceux-ci n'effectuant pas toute leur activité dans un même lieu, la difficulté du contrôle du nombre total de mammographies effectuées risque de compromettre considérablement leur recrutement. Enfin, dans le cadre du renforcement de la qualité de la prise en charge des tumeurs mammaires, la note du 3 novembre 2003 prévoit que les établissements hospitaliers de grande taille (CHU et CHR) et les CRLCC renforcent leur place en tant que structures permettant d'assurer une thérapie basée sur une décision pluridisciplinaire (radiologue, oncologue, chirurgien, anatomopathologiste...). De plus, ces structures sont en mesure de proposer un niveau de qualité des soins maximal en garantissant en particulier la mise en œuvre des bonnes pratiques chirurgicales définies par l'ANAES [Agence nationale d'accréditation et d'évaluation en santé 2002]. L'importance des coûts engagés dans la mise en place généralisée du programme de dépistage organisé du cancer du sein ne peut se justifier que si le dépistage individuel, traditionnellement important en France, disparaît au profit du dépistage organisé. Or, on constate que cette substitution est difficile y compris dans les départements pilotes pour la mise en place du dépistage organisé. Une substitution effective et suffisante du dépistage individuel par le dépistage organisé repose essentiellement sur les médecins et dans le respect de l'accord de bon usage des soins. Elle conditionnera à l'avenir l'intérêt de la poursuite des investissements faits dans le cadre du programme de dépistage organisé. Actuellement, la mammographie analogique reste la seule technique utilisable dans le cadre du programme de dépistage organisé. D'autres techniques, telles que l'imagerie par résonance magnétique ou l'échographie haute fréquence sont actuellement en cours d'évaluation. Elles pourraient avoir un intérêt comme examen d'appoint dans les situations où la mammographie conventionnelle est peu performante (seins denses, seins avec prothèse, femmes à risque génétique...). Actuellement, la supériorité de ces techniques en termes de détection sur la mammographie analogique n'est pas démontrée et les résultats des différentes études publiées jusqu'à ce jour divergent [International Agency for Research on Cancer 2002]. Un essai américain, actuellement en cours, dont les résultats sont prévus pour 2004-2005, permettra peut-être de trancher la question. Déjà en 2000, l'introduction de la mammographie numérique dans le programme de dépistage semblait inéluctable [Agence nationale d'accréditation et d'évaluation en santé 2000] même si son utilisation était encore en cours d'évaluation. Depuis, des études récemment publiées montrent que cette technique permet une réduction significative de la dose d'exposition aux rayons X [Gennaro 2004] et qu'elle permettrait une meilleure sensibilité lors de la détection des microcalcifications [Fischer 2002]. Par ailleurs, pour toute anomalie confondue, aucune différence significative de sensibilité n'a pu être mise en évidence entre la mammographie numérique et la mammographie conventionnelle [Lewin 2002, Skaane 2003]. La DGS étudie actuellement un projet d'expérimentation concernant l'utilisation de la mammographie numérique dans le cadre du programme national de dépistage. Il apparaît d'ores et déjà, que l'utilisation de la mammographie numérique serait avantageuse au niveau organisationnel puisqu'elle permettrait une simplification de la transmission des clichés (par exemple vers un centre de relecture), et de leur archivage. L'utilisation associée d'un logiciel de lecture assistée par ordinateur est également en cours d'évaluation. Cependant, malgré ces avantages organisationnels, la possibilité d'utiliser la mammographie numérique est toujours en attente de la mise en place du contrôle de qualité. Enfin, un des principaux inconvénients de ces appareils reste leur coût, de ce fait le passage au numérique ne sera pas réalisable dans tous les centres de radiologie. A plus long terme, une autre stratégie de dépistage du cancer du sein basée sur des analyses de biologie moléculaire pourrait voir le jour. Le principe est de détecter des variations d'activité d'un groupe de gènes spécifique de la maladie. Actuellement, une firme norvégienne, DiaGenic, est capable de mettre en évidence la variation d'expression de 49 gènes chez un groupe de femmes atteintes de cancer du sein. La spécificité de ce groupe de gènes vis-à-vis du cancer du sein reste à démontrer mais ce type de méthode présente l'avantage de permettre une détection très précoce et d'être basée sur un simple examen sanguin. Cet examen réduirait alors considérablement les besoins en mammographie et donc en mammographes et en radiologues. Par ailleurs, certaines équipes développent des méthodes de classification des tumeurs selon l'expression ou non d'un groupe de gènes associés à des pronostics différents [Bertucci 2003]. Les résultats de ces analyses pourraient orienter plus spécifiquement la stratégie thérapeutique proposée aux patientes. Grâce aux importants moyens déployés par le ministère de la santé, de la famille et des personnes handicapées dans le cadre du Plan cancer, l'objectif de généraliser les structures de dépistage organisé du cancer du sein sera vraisemblablement atteint à la fin de l'année 2004. A cette date, l'état de mise en place du programme de dépistage du cancer demeure néanmoins très hétérogène d'un département à l'autre, en partie parce que pour les deux tiers des départements le début de cette mise en place date de moins de 1 an. Il est, par ailleurs, important de comprendre que l'objectif réel à atteindre n'est pas la généralisation de la mise en place des structures de gestion mais l'obtention d'un taux de participation d'au moins 70 % parmi les femmes âgées de 50 à 74 ans. Début 2004, nous n'avons pas assez de recul pour avoir les premières évaluations de la mise en œuvre du cahier des charges actuel. Dans ces conditions, les résultats dont on dispose ne reflètent que partiellement la situation actuelle. Pour cette raison, il serait important pour l'utilisation de ce rapport dans le cadre des discussions parlementaires concernant le projet de loi sur le financement de la sécurité sociale 2005, de disposer de la mise à jour de certains résultats. A l'avenir, il apparaît essentiel que les délais de publication des résultats du programme de dépistage soient raccourcis afin qu'ils deviennent de véritables outils pour suivre et éventuellement ajuster la mise en place du programme. Malgré ces contraintes, certaines recommandations, regroupées sous quatre thématiques, peuvent d'ores et déjà être formulées. Mise en place du programme de dépistage - Favoriser la substitution du dépistage individuel par le dépistage organisé en limitant, à partir de 2006, le remboursement par l'assurance maladie aux seules mammographies de dépistage effectuées dans le cadre du programme national de dépistage organisé ou justifiée médicalement pour cause de risque génétique présenté par la patiente (mammographie avant 50 ans ou à un rythme supérieur à une fois tous les deux ans). Pour les autres mammographies de dépistage, le remboursement doit être de 0 %. - Inciter les radiologues à informer la structure de gestion de leur département chaque fois qu'ils réalisent une mammographie de dépistage chez une femme âgée de 50 à 74 ans en dehors du programme de dépistage organisé afin de combler les lacunes du fichier de l'assurance maladie et que cette dernière entre à l'avenir dans le programme de dépistage organisé. - Demander à la DGS, en lien avec l'AFSSAPS, de surveiller l'état du parc de mammographes agréés pour le programme de dépistage afin de connaître les conditions d'accès au dépistage et de prendre éventuellement les mesures nécessaires pour combler des pénuries locales d'équipement. - Soutenir les actions locales ciblées à destination des populations exclues du dépistage. - Améliorer la qualité de l'information vis-à-vis des femmes en présentant systématiquement les avantages et limites du dépistage. - Prévoir une information spécifique vis-à-vis des femmes se présentant au dépistage organisé pour améliorer leur fidélisation. - Poursuivre la diffusion d'information auprès des médecins (généralistes, gynécologues) pour qu'ils soient des médiateurs efficaces de la participation des femmes au programme de dépistage. - Soutenir les initiatives facilitant l'accès au dépistage dans les régions pauvres en équipement mammographique (mammobiles, organisation du transport vers les centres de radiologie). - Anticiper l'augmentation prévisible du nombre de mammographies réalisées annuellement en France au niveau des cabinets de radiologie. De même, évaluer et anticiper les besoins en personnel dans les structures de gestion associée à l'augmentation escomptée de la participation des femmes. - Rediscuter les conditions de participation au programme de dépistage des médecins des grands centres hospitaliers spécialisés dans le diagnostic en concertation avec les radiologues libéraux. - Améliorer la communication et la coopération entre le comité national de pilotage et les acteurs locaux en particulier les médecins coordonnateurs des structures de gestion. Assurance de qualité du programme de dépistage - Favoriser une démarche d'assurance de qualité au niveau du recueil des données anatomopathologiques. - Organiser les réseaux d'anatomocytopathologistes au niveau régional plutôt qu'au niveau départemental. - Favoriser la diffusion des bonnes pratiques chirurgicales établies par l'ANAES. - Favoriser l'utilisation du mammotome par son remboursement pour diminuer le nombre de biopsies inutiles au bloc opératoire. Evaluation du programme de dépistage - Utiliser en priorité les taux de participation et de fidélisation des femmes aux campagnes successives de dépistage pour évaluer le programme national. - Proposer rapidement un calendrier aboutissant à la standardisation de la définition des principaux indicateurs d'efficacité au niveau national (méthode de la mesure de la taille des tumeurs, critères anatomocytopathologiques des cancers invasifs). - Augmenter les moyens financiers et humains à disposition des registres pour améliorer la qualité des informations recueillies par ceux-ci. - Cibler les efforts pour obtenir une évaluation approfondie des résultats du programme de dépistage (mortalité par cancer du sein, cancers de l'intervalle, stades au diagnostic, faux négatifs, faux positifs) dans quelques départements possédant déjà un registre et une évaluation plus globale dans les autres départements en ne retenant que les indicateurs essentiels (taux de participation, taux de fidélisation, taux de cancers détectés). - Donner à l'InVS les moyens d'effectuer dans de meilleures conditions les évaluations annuelles du programme de dépistage, en particulier de réduire le délai de publication des données. Permettre l'ouverture de postes pérennes à l'InVS. - Permettre la réalisation d'audit des fonctionnements locaux pour homogénéiser l'organisation des programmes départementaux. - Permettre l'exploitation par l'InVS des données recueillies par les organismes d'assurance maladie et par l'observatoire de sénologie. - Mettre en place des études du rapport coût-efficacité dans quelques départements représentatifs. - Mettre en place des études sur l'impact du dépistage chez les femmes à risque en utilisant les données recueillies par l'observatoire de sénologie. Recherches à mener - Favoriser les recherches de biologie moléculaire à l'échelle européenne étudiant les différences entre les carcinomes canalaires in situ évolutifs de ceux qui ne le sont pas dans l'espoir de mettre en évidence un critère opérationnel utilisable en routine pour différencier ces deux types de tumeurs et donc de ne pas traiter inutilement les tumeurs non invasives. - Mettre en place des études évaluant l'impact du dépistage chez les femmes âgées de plus de 70 ans. Il sera essentiel de refaire un bilan de l'état de mise en place du programme de dépistage organisé lorsque les données de 2002 puis de 2004 seront disponibles pour vérifier en particulier l'amélioration des taux de participation et de fidélisation, la réduction du taux de perdues de vue et du délai de prise en charge. - ANNEXE 1 : Bibliographie - ANNEXE 2 : Composition de l'office - ANNEXE 3 : Composition du conseil des experts - ANNEXE 4 : Compte rendu de la réunion de l'office du 2 juin 2004. - Agence nationale d'accréditation et d'évaluation en santé. Le dépistage du cancer du sein par mammographie dans la population générale. 1999. - Agence nationale d'accréditation et d'évaluation en santé. Evaluation clinique de la numérisation en mammographie pour le diagnostic et le dépistage du cancer du sein. 2000. - Agence nationale d'accréditation et d'évaluation en santé. Chirurgie des lésions mammaires : prise en charge en première intention. 2002. - Agence nationale d'accréditation et d'évaluation en santé. Dépistage du cancer du sein par mammographie : évaluation de la méta-analyse de Gotzsche et Olsen 2002. - Ancelle-Park, R. Dépistage organisé du cancer du sein. Bulletin d'épidémiologie hebdomadaire 4, 13-28. 21-1-2003. - Anttinen I, Pamilo M, Soiva M, Roiha M. Double reading of mammography screening films--one radiologist or two?[comment]. Clinical Radiology 1993 ; 48: 414-421. - Arveux P, Wait S, Schaffer P. Building a model to determine the cost-effectiveness of breast cancer screening in France. European Journal of Cancer Care 2003 ; 12: 143-153. - Barr J, Francks A, Lee N, Herther P, Schachter M. Factors associated with continued participation in mammographiy screening. Prev.Med. 2001 ; 33: 661-667. - Barratt A, Irwig L, Glasziou P, Salkeld G, Houssami N. Benefits, harms and cost of screening mammography in women 70 years and over : a systematic review. MJA 2002 ; 176: 266-272. - Bertucci F, Viens P, Hingamp P, Nasser V, Houlgatte R, Birnbaum D. Breast Cancer revisited using DNA array-based gene expression profiling. Int.J.Cancer 2003 ; 103: 565-571. - Bonadona V, Lasset C. Prédispositions héréditaires au cancer du sein : après BRCA1 et BRCA2, quel(s) autre(s) gène(s) ? Bulletin du Cancer 2003 ; 90: 587-594. - Brancato B, Ciatto S, Bricolo D et al. [The assessment of the impact of a double reading by expert readers in a mass mammographic study]. Radiologia Medica 2000 ; 100: 21-23. - Brekelmans C, Seynaeve C, Bartels C et al. Effectiveness of breast cancer surveillance in BRCA1/2 gene mutation carriers and women with high familial risk. J. Clin. Oncol. 2001 ; 19: 924930. - Brown J, Bryan S, Warren R. Mammography screening : an incremental cost effectiveness analysis of double versus single reading of mammograms. British Medical Journal 1996 ; 312: 809-812. - Chamot E, Perneger T. The gynecologist's role in mammography screening in absence of a public health program. Arch.Gynecol.Obstet. 2003 ; 268: 88-93. - Ciatto S, Del Turco MR, Morrone D et al. Independent double reading of screening mammograms. Journal of Medical Screening 1995 ; 2: 99-101. - Daurès J-P, Guizard A-V, Séguret F, Nègre M, Delande G, Lamarque J-L et al. Estimation du bénéfice apporté par le dépistage de masse du cancer du sein dans le département de l'Hérault. Journal d'Economie Médicale 1998 ; 16 : 203-220. - Eisinger F, Alby N, Brémond A et al. Expertise collective INSERM-FNCLCC : recommandations portant sur la prise en charge des femmes ayant un risque génétique de développer un cancer du sein et/ou de l'ovaire. Bulletin du Cancer 1999 ; 86: 307-313. - Fischer U, Baum F, Obenauer S et al. Comparative study in patients with microcalcifications: fullfield mammography vs screen-film mammography. 2002 ; 12(11): 2679-2683. - Gennaro G, Baldelli P, Taibi A et al. Patient dose in full-field digital mammography : an italian survey. European Radiology 2004 ; 14(4): 645-652. - Gotzsche PC, Olsen O. Is screening for breast cancer with mammography justifiable?[comment]. Lancet 2000 ; 355: 129-134. - Goyder E, Barratt A, Irwig L. Telling people about screening programmes and screening test results: how can we do it better ? Journal of Medical Screening 2000 ; 7: 123-126. - Hill C. Intérêt du dépistage systématique des cancers du sein chez les femmes de plus de 70 ans. Bulletin du Cancer 2004 ; à paraître. - Humphrey L, Helfand M, Chan B, Woolf S. Breast cancer screening : a summary of the evidence for the US Preventive Services Task Force. Annals of Internal Medicine 2002 ; 137: 347-360. - Huo Z, Giger ML, Olopade OI et al. Computerized analysis of digitized mammograms of BRCA1 and BRCA2 gene mutation carriers. Radiology 2002 ; 225: 519-526. - Institut national de veille sanitaire. Dépistage du cancer du sein. 31-12-2000. - International Agency for Research on Cancer. Breast Cancer Screening. Lyon, France : 2002. - Jonsson H, Törnberg S, Nystrom L, Lenner P. Service screening with mammography of women aged 70-74 years in Sweden. Effects on breast cancer mortality. Cancer Detection and Prevention 2003 ; 27 : 360-369. - Kollias J, Sibbering D, Blamey R et al. Screening women aged less than 50 years with a family history of breast cancer. European Journal of Cancer 1998 ; 34 : 878-883. - Kuhl C, Schmutzler R, Kempe A et al. Breast MR Imaging screening in 192 women proved or suspected to be carriers of a breast cancer susceptibility gene : preliminary results. Radiology 2000 ; 215 : 267-279. - Lalloo F, Boggis C, Evans D, Shenton A, Threlfall A, Howell A. Screening by mammography, women with a family history of breast cancer. European Journal of Cancer 1998 ; 34 : 937-940. - Lasset C, Bonadona V. Prise en charge des femmes à risque héréditaire de cancer du sein : indications et modalités du dépistage par mammographie. Bulletin du Cancer 2001 ; 88 : 677-686. - Lauver D, Owen B, Egan J, Lovejoy L, Henriques J. Relationships of practitioner communications and characteristics with women's mammography use. Patient Educ.Couns. 2003 ; 51 : 65-74. - Leach MO, Eeles RA, Turnbull LW et al. The UK national study of magnetic resonance imaging as a method of screening for breast cancer (MARIBS). Journal of Experimental & Clinical Cancer Research 2002 ; 21 : 107-114. - Leivo T, Salminen T, Sintonen H et al. Incremental cost-effectiveness of double-reading mammograms. Breast Cancer Research & Treatment 1999 ; 54 : 261-267. - Lewin JM, D'Orsi CJ, Hendrick RE et al. Clinical comparison of fuull-field digital mammography and screen-film mammography for detection of breast cancer. AJR Am. J. Roentgenol. 2002 ; 179(3) : 671-677 - Mackay J, Rogers C, Fielder H et al. Development of a protocol for evaluation of mammographic surveillance services in women under 50 with a family history of breast cancer. Journal of Epidemiology & Biostatistics 2001 ; 6 : 365-369. - Mandelblatt J, Somnath S, Teutsch S et al. The cost-effectiveness of screening mammography beyond age 65 years: a systematic review for the U.S. Preventive Services Task Force. Annals of Internal Medicine 2003 ; 139 : 835-842. - Marshall T, Adab P. Informed consent for breast screening : what should we tell women ? Jounal of Medical Screening 2003 ; 10 : 22-26. - Maxwell C, Bancej C, Snider J. Predictors of mammography use among Canadian women aged 50-69: findings from the 1996/97 national population health study. CMAJ 2001 ; 164 : 329-334. - Niel, X. La démographie médicale à l'horizon 2020 : une réactualisation des projections à partir de 2002. 161. 2002. DREES. Etudes et résultats. - Nystrom L, Andersson I, Bjurstam N, Frisell J, Nordenskjold B, Rutqvist LE. Long-term effects of mammography screening: updated overview of the Swedish randomised trials.[comment][erratum appears in Lancet 2002 Aug 31 ; 360 (9334) : 724]. [Review] [15 refs]. Lancet 2002 ; 359 : 909-919. - Olsen O, Gotzsche PC. Cochrane review on screening for breast cancer with mammography. Lancet 2001a ; 358 : 1340-1342. - Olsen O, Gotzsche PC. Screening for breast cancer with mammography. Cochrane Database of Systematic Reviews 2001b ; CD001877. - Ottos SJ, Fracheboud J, Looman CWN et al. Initiation of population-based mammography screening in Dutch municipalities and effect on breast-cancer mortality : a systematic review. Lancet 2003 ; 361 : 1411-1417 - Remontet L, Esteve J, Bouvier AM et al. Cancer incidence and mortality in France over the period 1978-2000. Revue d Epidemiologie et de Sante Publique 2003 ; 51 : 3-30. - Séradour B, Wait S, Jacquemenier J et al. Modalities of reading of detection mammographies of the programme in the Bouches-du-Rhône. Results and costs 1990-1995. Journal of Radiology 1997 78(1) : 49-54. - Séradour B. Le programme de dépistage français : historique et nouvelles modalités. In: Séradour B, editor. Le dépistage du cancer du sein : un enjeu de santé publique. Paris: Springer, 2004 : 5966. - Skaane P, Young K, Skjennald A. Population-based mammography screening: comparison of screen-film and full-field digital mammography with soft-copy reading-Oslo I study. Radiology 2003 ; 229(3) : 877-884. - Smith-Bindman R, Chu PW, Miglioretti DL et al. Comparison of screening mammography in the United States and the United Kingdom. JAMA 2003 ; 290 : 2129-2137. - Thurfjell EL, Lernevall KA, Taube AA. Benefit of independent double reading in a populationbased mammography screening program. Radiology 1994 ; 191 : 241-244. - Van Ineveld B, Van Oortmarssen G, De Koning H, Boer R, Van der Maas P. How cost-effective is breast cancer screening in different EC countries ? Eur.J.Cancer 993 ; 29A : 1663-1668. - Wait S, Schaffer P, Seradour B et al. Le coût du dépistage du cancer du sein en France. J.Radiol. 2000 ; 81 : 799-806. - Wald N, Murphy P, Major P, Parkes C, Townsend J, Frost C. UKCC-CR multicentre randomised controlled trial of one and two view mammography in breast cancer screening. British Medical Journal 1995 ; 311 : 1189-1193. - Warner E, Plewes DB, Shumak RS et al. Comparison of breast magnetic resonance imaging, mammography, and ultrasound for surveillance of women at high risk for hereditary breast cancer. Journal of Clinical Oncology 2001 ; 19 : 3524-3531. - Zappa M, Visioli C, Ciatto S. Mammography screening in elderly women : efficacy and costeffectiveness. Critical reviews in Oncology/Hematology 2003 ; 46 : 235-239.
- Mme Claudine BLUM-BOISGARD, professeur de santé publique à l'Université Paris V et médecin conseil national de la Caisse nationale d'assurance maladie ; - M. Gérard BRÉART, professeur d'épidémiologie à l'Université Paris VI et directeur d'une unité de recherches de l'INSERM en santé périnatale et santé des femmes ; - Mme Françoise FORETTE, professeur de gériatrie à l'hôpital Broca et auteur de nombreux travaux sur la maladie d'Alzheimer ; - M. Claude LE PEN, professeur d'économie de la santé à l'Université Paris IX Dauphine et membre du laboratoire d'économie et de gestion des organisations de santé (LEGOS) ; - M. Arnold MUNNICH, professeur de génétique à l'Université Paris V et directeur d'une unité de recherche de l'INSERM ; - M. Thierry PHILIP, professeur de cancérologie à l'Université de Lyon et ancien président de la Fédération des centres de lutte contre le cancer. COMPTE RENDU DE LA RÉUNION L'office s'est réuni, le mercredi 2 juin 2004, au Sénat, sous la présidence de M. Nicolas About, sénateur, président, afin d'entendre les résultats de la saisine relative au dépistage du cancer du sein. M. Marc Bernier, rapporteur, a rappelé que l'objectif du rapport était d'évaluer le dispositif de dépistage du cancer du sein mis en place par les pouvoirs publics et d'émettre des propositions concrètes susceptibles d'améliorer la pertinence et l'efficacité du dispositif. Une réunion de travail à Marseille, le 10 septembre 2003, a permis de cibler les travaux des experts. Après la présentation de l'étude par M. Alain Brémond, professeur de médecine, expert auprès de la Fédération nationale des centres de la ligue contre le cancer, coordonnateur de l'étude consacrée au dépistage du cancer du sein, un débat s'est engagé. M. Marc Bernier, rapporteur, s'est interrogé sur les moyens qui pourraient être employés afin de faire accéder au système médical les femmes qui ne participent pas aujourd'hui au programme de dépistage. M. Alain Brémond a reconnu la réalité de ce problème et a évoqué plusieurs pistes, notamment une sensibilisation accrue à ces questions des médecins de terrain et des travailleurs sociaux. Il a considéré que la solution résidait dans le recours à plusieurs canaux de communication. M. Jean-Michel Dubernard, député, premier vice-président, a considéré qu'une partie des points évoqués par le rapport avait vocation à être prise en charge par l'Institut national du cancer (INCa) et s'est interrogé sur la distinction à faire entre les éléments à inclure dans le Plan cancer et les autres, notamment ceux devant faire l'objet d'une action des parlementaires. M. Alain Brémond a considéré que l'action publique devait prioritairement s'attacher à pérenniser le financement des centres de dépistage afin de leur faire bénéficier d'un personnel de qualité. M. Nicolas About, sénateur, président, s'est félicité de la généralisation du dépistage et a souhaité savoir si les examens pratiqués étaient désormais moins invasifs et moins agressifs pour les femmes. M. Alain Brémond a souligné qu'il s'agissait là d'une préoccupation fondamentale pour tout le personnel médical mais que, malheureusement, même si les effets secondaires étaient limités, l'examen demeurait peu agréable pour les patientes. En tous les cas, il faut évidemment éviter les opérations chirurgicales inutiles. M. André Vantomme, sénateur, a fait part de ses réserves sur la délimitation d'une fourchette d'âge de 50 à 74 ans pour la généralisation des dépistages et s'est interrogé sur les éventuels effets pervers d'un tel dispositif. Il a, par ailleurs, voulu connaître l'état d'équipement des centres spécialisés et de diffusion des nouvelles technologies. M. Alain Brémond a précisé que les études statistiques disponibles menées sous l'autorité de l'Agence nationale d'accréditation et d'évaluation en santé (ANAES) ne faisaient pas apparaître l'intérêt d'un dépistage systématique des femmes âgées de moins de 49 ans car ce dépistage ne se traduisait pas par une réduction du taux de mortalité dans ces tranches d'âge. Il a, par ailleurs, regretté que la diffusion des nouvelles technologies, notamment la tomographie à émission de positons, ne connaisse pas un rythme plus rapide. M. Jean Bardet, député, s'est interrogé sur les justifications de l'organisation du dépistage sur une base de deux ans. Il a également voulu savoir si la systématisation de la deuxième lecture permettait d'éliminer des diagnostics positifs posés à l'occasion de la première lecture. M. Alain Brémond a précisé que le cahier des charges transmis aux centres de dépistage ne prévoit une deuxième lecture systématique que des diagnostics positifs dès la première lecture, ce afin de ne pas retarder la prise en charge des patients. En outre, les mammographies ne sont plus archivées dans les centres de gestion, ce qui pose à la fois un problème médical en cas de diagnostic erroné et un problème scientifique puisque les erreurs ne pouvaient pas être analysées. Le délai de deux ans entre deux examens de dépistage relève plus d'un consensus autour des pratiques médicales que d'une nécessité établie scientifiquement. Mme Françoise Forette, membre du comité d'experts, a fait part de ses inquiétudes sur les conclusions de l'étude, notamment sur son impact pour les femmes de plus de 70 ans. M. Nicolas About, sénateur, président, s'est également interrogé sur les raisons scientifiques qui justifient que le dépistage serait moins utile après 70 ans. M. Alain Brémond a préconisé d'arrêter les invitations de dépistage adressées à ces femmes et a indiqué que les raisons principales étaient à rechercher du côté des patientes qui, à partir d'un certain âge, n'ont plus les mêmes préoccupations médicales. D'autres problèmes de santé interfèrent dans leur décision de pratiquer un examen de dépistage. M. Gilbert Barbier, sénateur, s'est interrogé sur la pertinence d'un remboursement des mammographies effectuées avant 50 ans. M. Alain Brémond a souligné que sa proposition de non-remboursement ne portait que sur les mammographies de dépistage non justifiées médicalement et a insisté à nouveau sur la nécessité de promouvoir les mammographies exécutées dans les centres de dépistage, dans le cadre d'un programme organisé. N° 1678 - Rapport sur les résultats du dépistage du cancer du sein (rapporteur : M. Marc Bernier) 1 Définition donnée par le site Internet de la Fédération nationale des centres de lutte contre le cancer (FNCLCC) : « Démarche consistant à rassembler les résultats de plusieurs essais cliniques conduits séparément sur un problème donné. Elle est justifiée par la disponibilité de données de qualité, provenant de différentes sources et dont les résultats ne concordent pas. Après vérification de la similitude des essais, il s'agit de réunir leurs résultats d'ensemble et de détail, en obtenant des responsables des études des informations individualisées et éventuellement mises à jour, pour les associer autant que possible et en tirer une conclusion globale dotée d'une signification statistique plus grande. » | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||